ÍNDUCE
- Esquemas
- Presentaciones
- Contenidos animados
- Concepto y clasificación de la materia.
- Propiedades de la materia.
- Propiedades generales: masa y volumen.
- Propiedades específicas o características. La densidad.
- Estados de agregación de la materia.
- Punto de vista macroscópico: forma y volumen.
- Punto de vista microscópico: teoría cinético-molecular de la materia.
- El estado gaseoso.
- Magnitudes que describen un gas.
- Leyes de los gases.
- Cambios físicos y químicos de la materia
- Cambios de estado. Gráficas de calentamiento y de enfriamiento.
- Concepto de mezcla. Tipos.
- Separación de los componentes de una mezcla.
- Separación de los componentes de mezclas heterogéneas.
- Filtración. 2.1.2.- Centrifugación.
- Decantación.
- Separación magnética.
- Tamizado.
- Separación de los componentes de mezclas homogéneas o disoluciones.
- Cristalización.
- Destilación.
- Disoluciones.
- Componentes y formación.
- Solubilidad.
- Concepto.
- Tipos de disoluciones.
- Curvas de solubilidad.
- Concentración de una disolución.
- Concepto.
- Formas de expresar la concentración.
- Porcentaje en masa.
- Porcentaje en volumen.
- Concentración en g/L.
1. ESQUEMAS


2. PRESENTACIONES






3. CONTENIDOS ANIMADOS




4. CONCEPTO Y CLASIFICACIÓN DE LA MATERIA
Si observamos a nuestro alrededor veremos materia por todas partes, desde el papel del libro que leemos hasta el agua que bebemos, pasando por el aire que respiramos. Todo lo que existe en la Naturaleza es materia. De una manera general, podemos definir la materia como todo aquello que tiene masa y que ocupa un cierto volumen en el espacio. Durante el desarrollo del tema intentaremos eliminar algunas ideas que podamos tener sobre la materia, como por ejemplo que es continua, que en la materia no existe el vacío, que es estática, etc.
La materia está en continuo cambio; en cualquier cambio que sufre la materia interviene “algo” a lo que se le llama energía. Así, decimos que la energía es una propiedad de la materia relacionada con la capacidad de producir cambios en ella misma o en otros sistemas materiales. Será estudiada con detenimiento más adelante durante este curso y en cursos posteriores.
Se denomina sistema material a un “trozo” o porción de materia que se considera de forma aislada para estudiarse con mayor facilidad. Si dicha porción de materia tiene una forma determinada se llama cuerpo. Además, no toda la materia es igual: a cada una de las distintas clases de materia que existen en la Naturaleza se le denomina sustancia. Por tanto, concluimos que todo lo que es materia estará formado por sustancias o por una mezcla de sustancias. Así, cualquier sistema material puede pertenecer a uno de los dos siguientes grupos:
- Sustancias puras: son aquellas que están formadas por un solo tipo de materia. Se clasifican a su vez en dos grandes grupos:
- Elementos: son aquellas sustancias puras que no pueden descomponerse en sustancias más sencillas por ningún método. Todos los elementos que existen en la Naturaleza aparecen en la tabla periódica, que estudiaremos más adelante. Ejemplos: oro, oxígeno, hierro, etc.
- Compuestos: son aquellas sustancias puras que sí se pueden descomponer en otras más sencillas por algún método. Los compuestos están formados por la unión de 2 o más elementos, y se representan mediante fórmulas químicas. Ejemplos: agua (H2O), dióxido de carbono (CO2), amoniaco (NH3), etc.
- Sustancias impuras o mezclas: son aquellas que están formadas por 2 o más tipos de materia. Pueden ser de 2 tipos:
- Mezclas homogéneas o disoluciones: son aquellas mezclas que tienen la misma composición y propiedades en todos sus puntos, es decir, no pueden distinguirse sus componentes a simple vista. Ejemplos: agua del mar, atmósfera, cocacola, etc.
- Mezclas heterogéneas: son aquellas mezclas que tienen diferente composición y propiedades en todos sus puntos, es decir, sus componentes pueden distinguirse a simple vista. Ejemplos: agua con arena, macarrones con tomate, etc.
5. PROPIEDADES DE LA MATERIA
Cualquier cuerpo o sistema material tiene unas ciertas propiedades que lo caracterizan. Estas propiedades pueden ser de 2 tipos:
5.1. PROPIEDADES GENERALES: MASA Y VOLUMEN
Las propiedades generales de la materia son aquellas que no nos permiten diferenciar unas sustancias de otras. Son la masa y el volumen:
5.1.1. La masa
La masa se define como la cantidad de materia que posee un cuerpo o sistema material. La cantidad de materia que tienen los cuerpos es independiente del estado de agregación en que se encuentran, es decir, dada una cierta masa de sustancia, ésta sigue siendo la misma si su estado es sólido, líquido o gaseoso. Su unidad en el S.I. es el kilogramo (kg), y se mide con balanzas, ya sean de platillos o digitales.
5.1.2. El volumen
El volumen se define como el espacio que ocupa un cuerpo o sistema material. Su unidad en el S.I. es el metro cúbico (m3 ), y suele medirse con pipetas o buretas si el cuerpo es líquido o con probetas si es sólido (mediante el método de inmersión). Si queremos medir el volumen de un sólido con forma geométrica regular, éste se calculará directamente mediante el uso de la fórmula adecuada (V = l3 para un cubo de lado l; V = π·r2 ·h para un cilindro de radio r y altura h; V = (4/3)·π·r 3 para una esfera de radio r, etc).
Sin embargo, medir el volumen de los gases no es tan sencillo, pues hay que tener en cuenta la presión y la temperatura a la que se encuentran; así, aunque los gases ocupan siempre el volumen del re - cipiente que los contiene, una misma masa de gas puede ocupar distintos volúmenes según la presión y temperatura a la que se encuentre. Esto no sucede ni con los sólidos ni con los líquidos.
5.1.2.1. Los cambios de volumen
Son dos:
Son dos:
- contracción
- dilatación.
Contracción.
Es la disminución de volumen que sufre un cuerpo al enfriarse.
Por ejemplo, los zapatos te quedan más "sueltos " en invierno; al poner un globo inflado en un tiesto con agua fría disminuye su tamaño.
La contracción se entiende porque al enfriarse los cuerpos, las partículas están más cercanas unas de otras, disminuye su movimiento y como consecuencia disminuye su volumen.
¿Qué ocurre cuando pones un termómetro en agua con hielo?
Dilatación.
Es el aumento de volumen que experimentan los cuerpos al contacto con la temperatura.
Por ejemplo, el Mercurio del termómetro se dilata con facilidad y por eso es capaz subir por un capilar pequeño e indicar el alza de temperatura.
Por ejemplo, el Mercurio del termómetro se dilata con facilidad y por eso es capaz subir por un capilar pequeño e indicar el alza de temperatura.
Este fenómeno no afecta sólo a los líquidos o sólidos también a los gases. Al recibir un aumento de calor, las partículas se separan entre sí, permitiendo que el gas se torne más liviano y se eleve. Ejemplo de esto es lo que hace posible que los "globos aerostáticos" se puedan elevar y desplazar.
Pero toda regla tiene su excepción y es el agua en este caso quién confirma la regla, porque al calentarse entre los 0º C y los 4º C, se contrae y al enfriarse se dilata. Se conoce este fenómeno como la dilatación anómala del agua.
5.2. PROPIEDADES ESPECÍFICAS O CARACTERÍSTICAS. LA DENSIDAD
Las propiedades específicas de la materia son aquellas que nos permiten diferenciar unas sustancias de otras, es decir, no existen dos sustancias diferentes que tengan el mismo valor de la misma propiedad específica. Algunas de ellas son la densidad, el punto de fusión y el de ebullición, etc. La más importante de ellas es la densidad, que estudiaremos a continuación. Decimos que la densidad es una propiedad específica de la materia porque no existen dos sustancias puras diferentes que tengan la misma densidad: cada sustancia pura tiene su valor propio de la densidad.
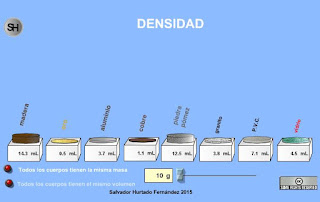
La densidad nos da idea de la cantidad de materia de cierta sustancia que existe en un cierto volumen de ella, es decir, la densidad es una magnitud (derivada) que relaciona la masa de un objeto con el volumen que ocupa. Se calcula de la siguiente manera:
La densidad de un líquido se mide con un aparato llamado densímetro, el cual se hunde más o menos en un líquido dependiendo de la sustancia que contenga en su interior. Para calcular la densidad de una sustancia sólida en el laboratorio se sigue el siguiente procedimiento:
- Se mide la masa del objeto con una balanza.
- Se mide el volumen del cuerpo por el método de inmersión: se mide un volumen de agua con la probeta, se sumerge el sólido y se anota el volumen final; el volumen del sólido será la resta o diferencia entre ambos.
- Dividimos la masa del objeto entre su volumen.
Ejemplo 3. Ejemplo práctico
Pesar el sólido seco (pequeñas bolitas de acero) en una balanza cuya precisión sea como mínimo de 0,1 g aunque son deseables precisiones de 0,01 g o inferiores

PESO DEL SÓLIDO__________ g.
Llenar hasta la mitad con agua el tubo de ensayo graduado y determinar el volumen de líquido introducido.

VOLUMEN INICIAL___________ml
Introducir el sólido pesado (las bolitas de acero) en el tubo de ensayo graduado.
Debes tener la precaución de que no queden burbujas de aire adheridas a la superficie del sólido.
Para ello golpea suavemente la base del tubo sobre un trapo depositado en la mesa.
Determina el nuevo volumen y anótalo en el cuaderno como volumen final.
VOLUMEN FINAL__________ml
El volumen del sólido será:
Volumen final - Volumen inicial.
Divide la masa del sólido por el volumen que has calculado y averigua en las tablas la naturaleza del sólido cuya densidad has calculado
Anota en un cuaderno todas las operaciones que hagas y los resultados que obtengas.
Densidad de algunas sustancias
Ejemplo 3. Ejemplo práctico
Pesar el sólido seco (pequeñas bolitas de acero) en una balanza cuya precisión sea como mínimo de 0,1 g aunque son deseables precisiones de 0,01 g o inferiores
| |
PESO DEL SÓLIDO__________ g. | |
Llenar hasta la mitad con agua el tubo de ensayo graduado y determinar el volumen de líquido introducido.
| |
VOLUMEN INICIAL___________ml
| |
Introducir el sólido pesado (las bolitas de acero) en el tubo de ensayo graduado.
| |
Determina el nuevo volumen y anótalo en el cuaderno como volumen final. | |
VOLUMEN FINAL__________ml
El volumen del sólido será: Volumen final - Volumen inicial. | |
Divide la masa del sólido por el volumen que has calculado y averigua en las tablas la naturaleza del sólido cuya densidad has calculado
| |
Anota en un cuaderno todas las operaciones que hagas y los resultados que obtengas.
| |
MATERIAL
|
DENSIDAD (g/cm3)
|
Oro
|
19,3
|
Plata
|
10,5
|
Cobre
|
8,9
|
Hielo
|
0,92
|
Madera de pino
|
0,50
|
Ejemplo 2. Considere una pepita de oro con una masa de 57,9 grs y volumen de 3 cm3. Obtenga su densidad.
- Puntos de fusión y de ebullición: serán estudiadas en el próximo tema.
- Dureza: es la propiedad que mide la resistencia de un sólido a ser rayado por otro sólido.
- Ductilidad: es una propiedad de los metales por la cual se pueden deformar y estirar en forma de hilos finos.
- Maleabilidad: es una propiedad de los metales por la cual se pueden deformar en forma de láminas.
- Compresibilidad: es una propiedad de los gases según la cual pueden reducir su volumen cuando se aumenta la presión sobre ellos.
- Viscosidad: es la propiedad que mide el grado de fluidez de un líquido. No debe confundirse con la densidad: por ejemplo, el agua es más densa que el aceite, pero menos viscosa.
PRÁCTICAS MATERIA








6. ESTADOS DE AGREGACIÓN DE LA MATERIA
Cualquier cuerpo o sistema material puede encontrarse en la Naturaleza de 3 maneras diferentes llamadas estados de agregación de la materia (o simplemente, estados de la materia): sólido, líquido y gaseoso. Las propiedades características de la materia (aunque sean del mismo tipo de materia) son diferentes en cada estado. Así, por ejemplo, el hielo es menos denso que el agua líquida. Podemos estudiar los estados de agregación desde dos puntos de vista diferentes:
6.1. PUNTO DE VISTA MACROSCÓPICO: FORMA Y VOLUMEN
Si observamos un cuerpo o sistema material a simple vista es muy fácil identificar si se trata de una sustancia sólida, líquida o gaseosa, ya que cada uno de estos estados tiene las siguientes propiedades:
 GAS
GAS
 LIQUIDO
LIQUIDO
 SOLIDO
SOLIDO



SÓLIDOS
LÍQUIDOS
GASES
COMPRESIBILIDAD No se pueden comprimir No se pueden comprimir Sí pueden comprimirse VOLUMEN Constante Constante Variable FORMA Constante Variable Variable
GRADOS DE LIBERTAD
Vibración Vibración, rotación y traslación restringidas Vibración, rotación, traslación EXPANSIBILIDAD No se expanden No se expanden Sí se expanden Fuerzas entre partículas Muy fuertes Fuertes Muy débiles Disposición de las partículas Ordenadas en posiciones fijas y cercanas Bastante desordenadas y cercanas Totalmente desordenadas y alejadas unas de otras
6.1.2. Estado sólido

Los sólidos se caracterizan por tener forma y volumen constantes. Esto se debe a que las partículas que los forman están unidas por unas fuerzas de atracción grandes de modo que ocupan posiciones casi fijas.
En el estado sólido las partículas solamente pueden moverse vibrando u oscilando alrededor de posiciones fijas, pero no pueden moverse trasladándose libremente a lo largo del sólido.
Las partículas en el estado sólido propiamente dicho, se disponen de forma ordenada, con una regularidad espacial geométrica, que da lugar a diversas estructuras cristalinas.
Al aumentar la temperatura aumenta la vibración de las partículas:
6.1.3. Estado líquido

Los líquidos, al igual que los sólidos, tienen volumen constante. En los líquidos las partículas están unidas por unas fuerzas de atracción menores que en los sólidos, por esta razón las partículas de un líquido pueden trasladarse con libertad. El número de partículas por unidad de volumen es muy alto, por ello son muy frecuentes las colisiones y fricciones entre ellas.
Así se explica que los líquidos no tengan forma fija y adopten la forma del recipiente que los contiene. También se explican propiedades como la fluidez o la viscosidad.
En los líquidos el movimiento es desordenado, pero existen asociaciones de varias partículas que, como si fueran una, se mueven al unísono. Al aumentar la temperatura aumenta la movilidad de las partículas (su energía).
6.1.4. Estado gaseoso

Los gases, igual que los líquidos, no tienen forma fija pero, a diferencia de éstos, su volumen tampoco es fijo. También son fluidos, como los líquidos.
En los gases, las fuerzas que mantienen unidas las partículas son muy pequeñas. En un gas el número de partículas por unidad de volumen es también muy pequeño.
Las partículas se mueven de forma desordenada, con choques entre ellas y con las paredes del recipiente que los contiene. Esto explica las propiedades de expansibilidad y compresibilidad que presentan los gases: sus partículas se mueven libremente, de modo que ocupan todo el espacio disponible. La compresibilidad tiene un límite, si se reduce mucho el volumen en que se encuentra confinado un gas éste pasará a estado líquido.
Al aumentar la temperatura las partículas se mueven más deprisa y chocan con más energía contra las paredes del recipiente, por lo que aumenta la presión:
Principales Características de los estados de la materia
SÓLIDOS
LÍQUIDOS
GASES
Poseen forma definida.
No poseen forma definida, por lo tanto adoptan la forma del recipiente que los contiene.
No poseen forma definida, por lo tanto adoptan la forma del recipiente que los contiene.
Poseen volumen fijo.
Poseen volumen fijo.
Poseen volumen variable.
Baja compresibilidad.
Compresión limitada.
Alta Compresibilidad.
En el estado sólido y en el estado líquido las sustancias pueden comportarse de formas muy distintas;
sin embargo, las sustancias gaseosas, aunque sean distintas, se comportan de forma parecida.
SÓLIDOS
|
LÍQUIDOS
|
GASES
| |
| COMPRESIBILIDAD | No se pueden comprimir | No se pueden comprimir | Sí pueden comprimirse |
| VOLUMEN | Constante | Constante | Variable |
| FORMA | Constante | Variable | Variable |
GRADOS DE LIBERTAD
| Vibración | Vibración, rotación y traslación restringidas | Vibración, rotación, traslación |
| EXPANSIBILIDAD | No se expanden | No se expanden | Sí se expanden |
| Fuerzas entre partículas | Muy fuertes | Fuertes | Muy débiles |
| Disposición de las partículas | Ordenadas en posiciones fijas y cercanas | Bastante desordenadas y cercanas | Totalmente desordenadas y alejadas unas de otras |
6.1.2. Estado sólido Los sólidos se caracterizan por tener forma y volumen constantes. Esto se debe a que las partículas que los forman están unidas por unas fuerzas de atracción grandes de modo que ocupan posiciones casi fijas. En el estado sólido las partículas solamente pueden moverse vibrando u oscilando alrededor de posiciones fijas, pero no pueden moverse trasladándose libremente a lo largo del sólido. Las partículas en el estado sólido propiamente dicho, se disponen de forma ordenada, con una regularidad espacial geométrica, que da lugar a diversas estructuras cristalinas. Al aumentar la temperatura aumenta la vibración de las partículas: 6.1.3. Estado líquido Los líquidos, al igual que los sólidos, tienen volumen constante. En los líquidos las partículas están unidas por unas fuerzas de atracción menores que en los sólidos, por esta razón las partículas de un líquido pueden trasladarse con libertad. El número de partículas por unidad de volumen es muy alto, por ello son muy frecuentes las colisiones y fricciones entre ellas. Así se explica que los líquidos no tengan forma fija y adopten la forma del recipiente que los contiene. También se explican propiedades como la fluidez o la viscosidad. En los líquidos el movimiento es desordenado, pero existen asociaciones de varias partículas que, como si fueran una, se mueven al unísono. Al aumentar la temperatura aumenta la movilidad de las partículas (su energía). 6.1.4. Estado gaseoso Los gases, igual que los líquidos, no tienen forma fija pero, a diferencia de éstos, su volumen tampoco es fijo. También son fluidos, como los líquidos. En los gases, las fuerzas que mantienen unidas las partículas son muy pequeñas. En un gas el número de partículas por unidad de volumen es también muy pequeño. Las partículas se mueven de forma desordenada, con choques entre ellas y con las paredes del recipiente que los contiene. Esto explica las propiedades de expansibilidad y compresibilidad que presentan los gases: sus partículas se mueven libremente, de modo que ocupan todo el espacio disponible. La compresibilidad tiene un límite, si se reduce mucho el volumen en que se encuentra confinado un gas éste pasará a estado líquido. Al aumentar la temperatura las partículas se mueven más deprisa y chocan con más energía contra las paredes del recipiente, por lo que aumenta la presión: |
Principales Características de los estados de la materia
SÓLIDOS
|
LÍQUIDOS
|
GASES
|
Poseen forma definida.
|
No poseen forma definida, por lo tanto adoptan la forma del recipiente que los contiene.
|
No poseen forma definida, por lo tanto adoptan la forma del recipiente que los contiene.
|
Poseen volumen fijo.
|
Poseen volumen fijo.
|
Poseen volumen variable.
|
Baja compresibilidad.
|
Compresión limitada.
|
Alta Compresibilidad.
|
6.2. PUNTO DE VISTA MICROSCÓPICO: TEORÍA CINÉTICO-MOLECULAR DE LA MATERIA
La teoría cinético-molecular de la materia intenta explicar el comportamiento de las sustancias teniendo en cuenta que éstas están formadas por partículas. Se basa en 3 ideas o postulados:
- Todas las sustancias están formadas por miles y miles de partículas muy pequeñas, no visibles a simple vista.
- Estas partículas se mueven en todas direcciones, chocando unas con otras y con las paredes del recipiente que las contiene.
- La velocidad a la que se mueven las partículas depende de la temperatura: a mayor temperatura, ma - yor velocidad.
- Cuando una sustancia se encuentra en estado sólido las partículas que la forman se encuentran muy juntas y apenas se mueven, debido a que entre ellas existen intensas fuerzas de atracción. Ello explica el hecho de que los sólidos tengan forma y volumen fijos.
- Si la sustancia se encuentra en estado líquido, las fuerzas de atracción entre las partículas es menor que en el caso anterior, lo cual les permite moverse a una cierta velocidad. Ello explica el que los líquidos tengan forma variable, la misma del recipiente que los contenga.
- En el estado gaseoso las fuerzas de atracción entre las partículas son prácticamente nulas, de modo que se podrán mover casi con total libertad y a grandes velocidades. Ello explica el hecho de que los gases (gas procede de la palabra griega chaos, que significa desorden o caos) tengan forma y volumen variables, además de poder fluir y difundirse con facilidad.
6.3.1. Magnitudes que describen un gas.
Cualquier gas se caracteriza por 3 magnitudes:
- Presión (p): nos indica la cantidad de choques de las partículas con las paredes del recipiente que contiene el gas. En las leyes de los gases se mide en atmósferas (atm), aunque también puede medirse en pascales (Pa) ó en mm de mercurio (mm de Hg); la equivalencia entre estas unidades es la siguiente:
1 atm = 101300 Pa = 760 mm de Hg
- Volumen (V): nos indica el espacio que ocupa el gas o bien el del recipiente que lo contiene. En la ecuación de los gases se expresa en litros.
- Temperatura (T): nos indica la velocidad a la que se mueven las partículas; a mayor temperatura, mayor velocidad. En la ecuación general de los gases se expresa en kelvin (K); su relación con el grado centígrado (ºC) es la siguiente:
T(K) = T(ºC) + 273
Las leyes de los gases son experimentales, es decir, han sido deducidas a partir de resultados obtenidos en el laboratorio. En orden cronológico, son las siguientes:
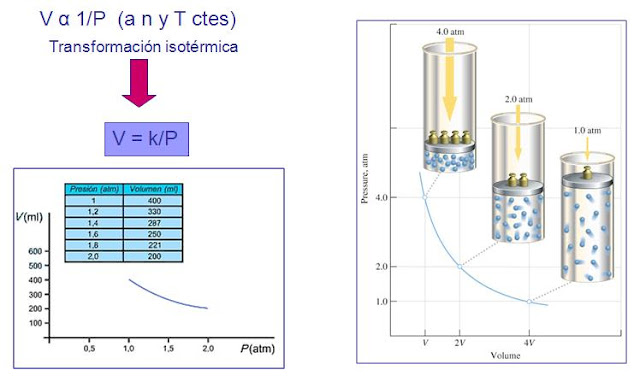
6.3.2.1. Ley de Boyle-Mariotte:
Fue establecida en 1662 de manera simultánea e independiente por el científico inglés Robert Boyle y por el francés E. Mariotte. Establece que si la temperatura de un gas permanece constante, su presión y su volumen son inversamente proporcionales (cuando uno aumenta, el otro disminuye, y viceversa), de manera que su producto permanece constante:
p.V = cte ⇒ p1.V1 = p2.V2
donde 1 y 2 son los estados inicial y final del gas (antes y después de la transformación que haya
sufrido). 

6.3.2.2. Ley de Charles:
Fue establecida en 1798. Establece que si la presión de un gas permanece constante, su volumen y su temperatura son directamente proporcionales, es decir, si aumenta la temperatura, también lo hará el volumen, y viceversa:
V / T = cte ⇒ V1 /T1 = V2/T2
Fue establecida en 1802. Establece que si el volumen de un gas permanece constante, la presión y la temperatura son directamente proporcionales:
p / T = cte ⇒ p1/ T1 = p2 /T2


7. CAMBIOS FÍSICOS Y QUÍMICOS DE LA MATERIA

Las modificaciones en la presión, la temperatura o las interrelaciones de las sustancias, pueden originar cambios físicos o químicos en la materia.
Son aquellos cambios que no generan la creación de nuevas sustancias, lo que significa que no existen cambios en la composición de la materia, como se ve en la figura siguiente.
| El cambio físico se caracteriza por la no existencia de reacciones químicas y de cambios en la composición de la materia. |
Cambio físico de la materia: cambio de estado sólido (hielo) a estado líquido del agua, mediante el aumento en la temperatura del sistema.
|
7.2. Cambios químicos:
Son aquellos cambios en la materia que originan la formación de nuevas sustancias, lo que indica que existieron reacciones químicas.
| El cambio Químico de la materia se caracteriza por la existencia de reacciones químicas, de cambios en la composición de la materia y la formación de nuevas sustancias. |
Cambio Químico de la materia: Formación de Ácido Clorhídrico, mediante la reacción de Cloro e Hidrógeno.
Los procesos físicos y químicos se diferncian fundamentalmente en:
| Aspecto | Cambio físico | Cambio químico |
| propiedades | Modificación pequeña y/o parcial de las propiedades | Modificación profunda en las propiedades |
| reversibles? | Son siempre reversibles | Por los general, son irreversibles |
| Energía | La energía puesta en juego en el cambio es pequeña | Se produce una gran variación de energía. |
PRÁCTICA
8. CAMBIOS DE ESTADO
Si la temperatura de un objeto aumenta o disminuye hasta un cierto valor, éste puede comenzar a
cambiar de estado de agregación. Los cambios de estado que pueda sufrir cualquier sustancia tienen lugar
siempre a una misma temperatura; además, mientras dure el cambio de estado la temperatura de ésta no
cambia hasta que no se haya transformado totalmente. Las dos temperaturas más importantes en los cambios
de estado son las siguientes:
- Punto de fusión: es la temperatura a la cual una sustancia pasa de estado sólido a líquido o viceversa.
- Punto de ebullición: es la temperatura a la cual una sustancia pasa de estado líquido a gaseoso o viceversa.
- Cambios de estado progresivos: son aquellos que se producen cuando la temperatura del objeto aumenta, esto es, cuando absorbe calor. Son la fusión, la vaporización y la sublimación o volatilización.
- Cambios de estado regresivos: son aquellos que se producen cuando la temperatura del objeto disminuye, esto es, cuando desprende calor. Son la condensación o licuefacción, la solidificación y la sublimación inversa o regresiva.
Debemos recordar que los cambio de estado es un proceso físico, ya que al terminar la sustancia sigue siendo la misma.
Conociendo los puntos de fusión y de ebullición, podemos dibujar las gráficas de calentamiento o de enfriamiento de cualquier sustancia, las cuales sirven para estudiar cómo cambia la temperatura de una sustancia conforme avanza el tiempo. En estas gráficas la temperatura se representa en el eje vertical y el tiempo, en el eje horizontal:
- Si la gráfica es de calentamiento, entonces tendrá forma creciente (de abajo hacia arriba). En los tramos inclinados la sustancia aumenta su temperatura (por tanto, en ellos se encontrará en estado sólido, líquido o gaseoso), mientras que en los tramos horizontales la temperatura de la sustancia permanece constante, lo cual significa que en ellos es donde tiene lugar el cambio de estado. Durante un cierto tiempo, la sustancia va transformándose progresivamente de un estado a otro. Hasta que no se transforma en su totalidad la temperatura no comienza a aumentar de nuevo.


- Si la gráfica es de enfriamiento, entonces tendrá forma decreciente (de arriba hacia abajo). En los tramos inclinados la sustancia disminuye su temperatura (por tanto, en ellos se encontrará en estado gaseoso, líquido o sólido), mientras que en los tramos horizontales la temperatura de la sustancia permanece constante, lo cual significa que en ellos es donde tiene lugar el cambio de estado. Durante un cierto tiempo, la sustancia va transformándose progresivamente de un estado a otro. Hasta que no se transforma en su totalidad la temperatura no comienza a descender de nuevo.
En el estado sólido las partículas están ordenadas y se mueven oscilando alrededor de sus posiciones. A medida que calentamos el agua, las partículas ganan energía y se mueven más deprisa, pero conservan sus posiciones.
Cuando la temperatura alcanza el punto de fusión (0ºC) la velocidad de las partículas es lo suficientemente alta para que algunas de ellas puedan vencer las fuerzas de atracción del estado sólido y abandonan las posiciones fijas que ocupan. La estructura cristalina se va desmoronando poco a poco. Durante todo el proceso de fusión del hielo la temperatura se mantiene constante.
En el estado líquido las partículas están muy próximas, moviéndose con libertad y de forma desordenada. A medida que calentamos el líquido, las partículas se mueven más rápido y la temperatura aumenta. En la superficie del líquido se da el proceso de vaporización, algunas partículas tienen la suficiente energía para escapar. Si la temperatura aumenta, el número de partículas que se escapan es mayor, es decir, el líquido se evapora más rápidamente.
Cuando la temperatura del líquido alcanza el punto de ebullición, la velocidad con que se mueven las partículas es tan alta que el proceso de vaporización, además de darse en la superficie, se produce en cualquier punto del interior, formándose las típicas burbujas de vapor de agua, que suben a la superficie. En este punto la energía comunicada por la llama se invierte en lanzar a las partículas al estado gaseoso, y la temperatura del líquido no cambia (100ºC).
En el estado de vapor, las partículas de agua se mueven libremente, ocupando mucho más espacio que en estado líquido. Si calentamos el vapor de agua, la energía la absorben las partículas y ganan velocidad, por lo tanto la temperatura sube.
Podemos explicar los cambios de estado desde un punto de vista microscópico, utilizando la teoría cinético-molecular de la materia. Vamos a distinguir entre los cambios de estado progresivos y los regresivos:
Tienen lugar cuando aumenta la temperatura de la sustancia. Sabemos
que entonces las partículas se mueven cada vez más rápido; en cuanto se alcanza el punto de
fusión, las partículas se mueven con tal rapidez que comienzan a disminuir las fuerzas de cohesión
entre ellas, de modo que la sustancia pasa a estado líquido. Todo el calor que la sustancia absorbe se
invierte en debilitar dichas fuerzas, lo cual explica que la temperatura permanezca constante en los
cambios de estado. Si la temperatura prosigue aumentando, las partículas se moverán aún más rápido
y se alcanzará el punto de ebullición; ahora el calor que absorbe la sustancia se invierte en debilitar
aún más las fuerzas de cohesión entre partículas, haciéndolas casi inexistentes: cuando todas ellas se
hayan debilitado, la sustancia se habrá transformado totalmente en estado gaseoso.
8.2. Los cambios de estado regresivos
Estos son: sublimación progresiva, fusión y evaporación.
Sublimación progresiva. Es la transformación directa, sin pasar por otro estado intermedio, de una materia en estado sólido a estado gaseoso al aplicarle calor. Ejemplo: Hielo (agua en estado sólido) + temperatura = vapor (agua en estado gaseoso) |
Fusión. Es la transformación de un sólido en líquido al aplicarle calor. Es importante hacer la diferencia con el punto de fusión, que es la temperatura a la cual ocurre la fusión. Esta temperatura es específica para cada sustancia que se funde. Ejemplos: Cobre sólido + temperatura = cobre líquido. Cubo de hielo (sólido) + temperatura = agua (líquida). El calor acelera el movimiento de las partículas del hielo, se derrite y se convierte en agua líquida. |
Sustancia
|
Punto de fusión (ºC)
|
Punto de ebullición (ºC)
|
Agua (sustancia)
|
0
|
100
|
Alcohol (sustancia)
|
-117
|
78
|
Hierro (elemento)
|
1.539
|
2.750
|
Cobre (elemento)
|
1.083
|
2.600
|
Aluminio (elemento)
|
660
|
2.400
|
Plomo (elemento)
|
328
|
1.750
|
Mercurio (elemento)
|
-39
|
357
|
Evaporación. Es la transformación de las partículas de superficie de un líquido, en gas, por la acción del calor. Este cambio ocurre en forma normal, a temperatura ambiente, en algunas sustancias líquidas como agua, alcohol y otras. Ejemplo. Cuando te lavas las manos y las pones bajo la máquina que tira aire caliente, éstas se secan. Sin embargo si le aplicamos mayor temperatura la evaporación se transforma en ebullición. |
Ebullición. Es la transformación de todas las partículas del líquido en gas por la acción del calor aplicado. En este caso también hay una temperatura especial para cada sustancia a la cual se produce la ebullición y la conocemos como punto de ebullición. Ejemplos: El agua tiene su punto de ebullición a los 100º C, alcohol a los 78º C. (el término hervir es una forma común de referirse a la ebullición). |
Tienen lugar cuando disminuye la temperatura de la sustancia. Sabemos
que si la sustancia se encuentra en estado gaseoso las partículas se mueven muy rápido; en
cuanto se alcanza el punto de ebullición, las partículas se mueven con mayor lentitud, de modo que
comienzan a aumentar las fuerzas de cohesión entre ellas: la sustancia pasa a estado líquido. Todo el
calor que la sustancia desprende se invierte en aumentar dichas fuerzas, lo cual explica que la tempe -
ratura permanezca constante en los cambios de estado. Si la temperatura prosigue disminuyendo, las
partículas se moverán aún más lentamente y se alcanzará el punto de fusión; ahora el calor que desprende
la sustancia se invierte en aumentar aún más las fuerzas de cohesión entre partículas, haciéndolas
muy intensas y disminuyendo casi totalmente la movilidad de las mismas: cuando todas ellas
hayan aumentado hasta que las partículas permanezcan casi inmóviles, fuertemente unidas entre
ellas, la sustancia se habrá transformado totalmente en estado sólido.
9. CONCEPTO DE MEZCLA. TIPOS.
Sabemos que cualquier sustancia material puede clasificarse en dos grandes grupos: sustancias puras y sustancias impuras o mezclas. A lo largo del tema estudiaremos éstas, que son aquellas que están formadas por 2 o más componentes que pueden mezclarse en cualquier proporción. Las mezclas pueden ser, a su vez, de 2 tipos:
10. SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA.
En muchísimos procesos industriales (industrias alimentaria, petrolífera, siderúrgica, etc.) es necesario separar los distintos componentes que forman parte de una mezcla, ya sea homogénea o heterogénea. En este apartado estudiaremos los métodos más importantes, agrupados según el tipo de mezcla de que se trate. Estos métodos son físicos, pues no alteran las sustancias que forman la mezcla.
10.1. SEPARACIÓN DE LOS COMPONENTES DE MEZCLAS HETEROGÉNEAS
10.1.1. FILTRACIÓN
La filtración sirve para separar una sustancia sólida no miscible (que no esté disuelta) con una sustancia líquida. Consiste en utilizar un filtro cuyos poros (o agujeros) son más pequeños que el tamaño de las partículas que se quiera separar, de manera que cuando la mezcla se haga pasar a través del filtro éstas quedarán retenidas. Esta técnica se utiliza para separar la nata de la leche, para tamizar la arena en las construcciones, etc.


10.1.2. CENTRIFUGACIÓN
Sirve para separar, habitualmente, suspensiones de sólidos en líquidos. Consiste en hacer girar la mezcla a una gran velocidad; de esta manera, las partículas más pesadas tienden a “escaparse” de la mezcla, separándose de las restantes. Lógicamente, cuanto mayor sea la masa, con mayor fuerza se separarán las partículas, que quedarán retenidas en el fondo del tubo. Esta técnica se utiliza en los laboratorios de análisis clínicos para separar y estudiar algunas de las sustancias (por ejemplo, los glóbulos rojos) que se encuentran en la sangre.


10.1.3. DECANTACIÓN
Sirve para separar dos o más líquidos inmiscibles entre ellos. El método se basa en las diferentes densidades de los líquidos que forman parte de la mezcla. Por ejemplo, en el caso de una mezcla de agua y aceite (ver figura a la derecha) el agua se sitúa por debajo debido a su mayor densidad; utilizando un embudo de decantación, abrimos la llave que se encuentra en la parte inferior y dejamos caer el agua; si cerramos la llave cuando vaya a caer el aceite, habremos conseguido separar ambos líquidos.
10.1.4. SEPARACIÓN MAGNÉTICA
Sirve para separar una sustancia que forme parte de la mezcla y que posea propiedades magnéticas, es decir, se vea atraída por un imán. Estas sustancias suelen ser metales. Acercando un imán a la mezcla, conseguiremos separar aquellas sustancias que se vean atraídas por él. Esta técnica suele utilizarse en las industrias siderúrgicas para separar los metales del mineral del que proceden.
10.1.5. TAMIZADO
Es el método indicado para separar los componentes de una mezcla de sólidos según el tamaño de sus partículas. Utilizando el tamiz apropiado, retendremos en él el sólido cuyas partículas sean más gruesas.

10.2. SEPARACIÓN DE LOS COMPONENTES DE MEZCLAS HOMOGÉNEAS O DISOLUCIONES
10.2.1. CRISTALIZACIÓN
Sirve para separar una sustancia (habitualmente sólida) que se encuentra disuelta en un líquido. Para ello, se utiliza un recipiente muy ancho llamado cristalizador (ver figura a la derecha), en el cual se vierte la disolución; entonces, si se deja evaporar lentamente, el agua va pasando a estado gaseoso y las partículas de la sustancia sólida se unen poco a poco formando cristales con formas geométricas definidas (rombos, polígonos, etc.). Un ejemplo de cristalización es la separación de la sal del agua del mar en las salinas. La cristalización se puede acelerar aún más mediante el calentamiento a sequedad, que consiste en calentar la disolución en una cápsula de porcelana (ver figura a la izquierda) que se pone en contacto con una fuente de calor (hornillo, mechero,...). En este caso, los cristales de sólido que se obtienen al evaporarse el líquido son de menor tamaño que los que se obtienen a partir de la cristalización.


10.2.2. DESTILACIÓN
Sirve para separar una mezcla de dos o más líquidos miscibles entre sí. Para ello, se utiliza un dispositivo como el de la izquierda: se introduce la mezcla de líquidos en el matraz y comienza a calentarse. Entonces, el líquido con menor punto de ebullición comenzará a evaporarse antes que los demás; el agua corre por el tubo refrigerante enfriando dicho vapor, transformándolo en estado líquido (condensación). El líquido termina por caer en el recipiente colector, separándose así del resto de la mezcla. Para que la destilación sea eficaz, los líquidos deben tener puntos de ebullición que se diferencien en, al menos, 10 ºC.


11. DISOLUCIONES.
11.1. COMPONENTES Y FORMACIÓN.
Una disolución es una mezcla homogénea formada por dos componentes:
El soluto y el disolvente pueden encontrarse en cualquiera de los 3 estados de agregación; en la tabla que aparece a continuación aparecen algunos ejemplos de disoluciones tomados de la vida cotidiana en los que el soluto y el disolvente aparecen en distintos estados de agregación. Esta tabla nos da una idea de la importancia de las disoluciones, pues multitud de sustancias naturales y artificiales se presentan de este modo; incluso casi todos los procesos biológicos que tienen lugar en el interior de los organismos vivos suceden entre sustancias disueltas en agua.
Hemos dicho al principio del apartado 1 que una disolución o mezcla homogénea tiene la misma composición y propiedades en todos sus puntos, es decir, que sus componentes no pueden distinguirse a simple vista. Podemos explicar esto a partir de la teoría cinético-molecular, aplicándolo al ejemplo de una disolución de sal (o cloruro de sodio) en agua: cuando se disuelve la sal en agua, los granos de sal son atraídos por las moléculas de agua, de modo que cada grano de sal se va fragmentando (o rompiendo) en partículas de cloro y de sodio, que son muy pequeñas e invisibles a simple vista. Ésta es la razón de que no podamos distinguir a simple vista los componentes de una disolución.
El volumen resultante de la mezcla entre el soluto y el disolvente no es aditivo, pues debido al reajuste de espacios entre las distintas partículas del soluto y del disolvente, el volumen final es inferior al de la suma de ellos (aunque en los ejercicios consideraremos que los volúmenes sí son aditivos). Sin embargo, la masa de la disolución resultante sí es aditiva, es decir, es igual a la suma de las masas de soluto y disolvente.
11.2. SOLUBILIDAD
11.2.1. CONCEPTO
No todas las sustancias se disuelven con la misma facilidad en un disolvente (por ejemplo, agua). A la cantidad máxima de soluto que puede disolverse en una cierta cantidad de disolvente a una cierta temperatura se le llama solubilidad de la sustancia. Así pues, la solubilidad de las sustancias depende de la temperatura y del estado de agregación en que se encuentre el soluto; así, tenemos:
A partir del concepto de solubilidad, podemos clasificar las disoluciones en varios tipos:
11.2.3. CURVAS DE SOLUBILIDAD
Las curvas de solubilidad son representaciones gráficas que nos permiten estudiar cómo varía la solubilidad de una sustancia en agua, ya sea dicha sustancia sólida, líquida o gaseosa, conforme varía (aumenta o disminuye) su temperatura. En el eje horizontal aparecen las temperaturas en ºC, y en el eje vertical aparece la solubilidad de la sustancia expresada generalmente en g de sustancia/100 g de agua (ó g de sustancia/100 ml de agua).
En la gráfica de la derecha aparece un ejemplo de dichas gráficas o curvas.
De ella deducimos que la solubilidad aumenta
cuando aumenta la temperatura. Asimismo, podemos saber qué cantidad máxima
de soluto podrá disolverse en agua para cada valor de la temperatura, o qué cantidad
no se disolvería (precipitaría) en caso de que la disolución se enfríe o se caliente
desde una temperatura a otra.
PRÁCTICA

11.3. CONCENTRACIÓN DE UNA DISOLUCIÓN.
11.3.1. CONCEPTO
La concentración de una disolución es una magnitud que nos indica la relación entre la cantidad de soluto que hay disuelta en una cierta cantidad de disolvente o de disolución. Así pues, la concentración nos indica cuál es la proporción entre soluto y disolvente o disolución. Obviamente, cuanto mayor sea su valor, más concentrada será la disolución; cuanto más pequeña sea la concentración, más diluida será. Ahora bien, el soluto que se disuelve se reparte por igual en toda la disolución, lo cual significa que la proporción entre soluto y disolvente no depende de la cantidad de disolución que se examine. Un ejemplo de lo dicho sucede si disolvemos dos cucharadas de azúcar en un vaso de leche: la leche estará igual de dulce si nos tomamos medio vaso, una cucharada o el vaso entero.
11.3.2. FORMAS DE EXPRESAR LA CONCENTRACIÓN
Existen muchas formas de expresar la concentración de una disolución. Este curso veremos sola - mente 3 de ellas: el porcentaje en masa, el porcentaje en volumen y la concentración expresada en g/l.

11.3.2.1. PORCENTAJE EN MASA
El porcentaje en masa de una disolución nos indica la relación entre la masa de soluto y la masa de disolución en que está disuelta. Se calcula de la siguiente manera:
Ejemplo: Preparamos una disolución que contiene 2 g de cloruro de sodio (NaCl) y 3 g de cloruro de potasio (KCl) en 100 g de agua destilada. Calcula el tanto por ciento en masa de cada soluto en la disolución obtenida.
Primeramente, se trata de identificar a los solutos y al disolvente. En este caso, el disolvente es el agua, pues es la sustancia que se encuentra en mayor proporción y los solutos serán NaCl y KCl. La masa de soluto será la que hay para cada uno de ellos; la masa de disolución es la suma de todas las masas de sustancias presentes en la mezcla: 2 g + 3 g + 100 g = 105 g. Por tanto:
Esto indica que si tuviésemos 100 g de disolución, 1,9 g serían de cloruro sódico, 2,8 g serían de cloruro potásico y el resto, hasta 100 g, serían de agua.

11.3.2.2. PORCENTAJE EN VOLUMEN
El porcentaje en volumen de una disolución relaciona el volumen de soluto con el volumen de disolución en que éste está disuelto. Se calcula de la siguiente manera:
Ejemplo: Preparamos una disolución añadiendo 5 ml de alcohol etílico junto a 245 ml de agua. Calcula el % en volumen de soluto en la disolución.
En este caso, el soluto es el alcohol pues está en menor cantidad y el disolvente es el agua. El volumen de disolución es la suma de volúmenes de los componentes (no tiene porqué ser así siempre): 5 ml + 245 ml = 250 ml. Por tanto:

11.3.2.3. CONCENTRACIÓN EN g/L
La concentración expresada en g/l de una disolución (abreviadamente la representaremos con la letra C) se define como la masa de soluto, expresada en gramos, que hay disuelta en el volumen de disolución, expresado en litros, en que está disuelto. Se calcula de la siguiente manera:

Estos cambios se producen por el enfriamiento de los cuerpos y también distinguimos tres tipos que son: sublimación regresiva, solidificación, condensación.
Sublimación regresiva. Es el cambio de una sustancia de estado gaseoso a estado sólido, sin pasar por el estado líquido. |
Solidificación. Es el paso de una sustancia en estado líquido a sólido. Este cambio lo podemos verificar al poner en el congelador un vaso con agua, o los típicos cubitos de hielo. |
Condensación. Es el cambio de estado de una sustancia en estado gaseoso a estado líquido. Ejemplo: El vapor de agua al chocar con una superficie fría, se transforma en líquido. En invierno los vidrios de las micros se empañan y luego le corren "gotitas"; es el vapor de agua que se ha condensado. En el baño de la casa cuando nos duchamos con agua muy caliente y se empaña el espejo, luego le corren las "gotitas " de agua. |
Sabemos que cualquier sustancia material puede clasificarse en dos grandes grupos: sustancias puras y sustancias impuras o mezclas. A lo largo del tema estudiaremos éstas, que son aquellas que están formadas por 2 o más componentes que pueden mezclarse en cualquier proporción. Las mezclas pueden ser, a su vez, de 2 tipos:
- Mezclas homogéneas o disoluciones: son aquellas que tienen la misma composición y propiedades en todos sus puntos, es decir, aquellas cuyos componentes no pueden distinguirse a simple vista, ni siquiera con un microscopio ordinario. Ello es lo que sucede cuando se disuelve azúcar en agua: una vez disuelto el azúcar, ya no puede diferenciarse del agua.
- Mezclas heterogéneas: son aquellas que tienen diferente composición y propiedades en todos sus puntos, es decir, aquellas cuyos componentes sí pueden distinguirse a simple vista. Es lo que sucede cuando se mezclan, por ejemplo, agua y arena.
DISPERSIONES COLOIDALES
Un caso intermedio entre las mezclas homogéneas y las mezclas heterogéneas son las dispersiones coloidales o coloides.
Las partículas de los coloides, también llamadas micelas tienen un tamaño superior a 10-7cm e inferior a 2 X 10-5 cm.
Con este tamaño, las micelas atraviesan los filtros ordinarios y son invisibles al microscopio, pero se ven en el ultramicroscopio y son retenidas por los poros de los ultrafiltros
La iluminación lateral de una dispersión coloidal produce el efecto Tyndall. El rayo de luz se hace visible al atravesar una dispersión coloidal (efecto en el que se basa el ultramicroscopio), pero no es visible cuando atraviesa una disolución verdadera. Esto se debe a que las partículas coloidales, por su tamaño, difunden la luz, mientras que las disueltas no lo hacen.
En la tabla tienes algunos ejemplos de dispersiones coloidales:
Tipos de coloides
| |||
| Partículas dispersas | Medio dispersante | Nombre | Ejemplos |
| gas | líquido | espuma | espuma de afeitar |
| gas | sólido | espuma sólida | corcho blanco |
| líquido | gas | aerosol líquido | niebla, bruma |
| líquido | líquido | emulsión | leche, mayonesa |
| líquido | sólido | gel | gelatina |
| sólido | gas | aerosol sólido | polvo, humo |
| sólido | líquido | sol | pinturas, látex |
| sólido | sólido | sol sólido | rubí , turquesa |
10. SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA.
En muchísimos procesos industriales (industrias alimentaria, petrolífera, siderúrgica, etc.) es necesario separar los distintos componentes que forman parte de una mezcla, ya sea homogénea o heterogénea. En este apartado estudiaremos los métodos más importantes, agrupados según el tipo de mezcla de que se trate. Estos métodos son físicos, pues no alteran las sustancias que forman la mezcla.
10.1. SEPARACIÓN DE LOS COMPONENTES DE MEZCLAS HETEROGÉNEAS
10.1.1. FILTRACIÓN
La filtración sirve para separar una sustancia sólida no miscible (que no esté disuelta) con una sustancia líquida. Consiste en utilizar un filtro cuyos poros (o agujeros) son más pequeños que el tamaño de las partículas que se quiera separar, de manera que cuando la mezcla se haga pasar a través del filtro éstas quedarán retenidas. Esta técnica se utiliza para separar la nata de la leche, para tamizar la arena en las construcciones, etc.


Sirve para separar, habitualmente, suspensiones de sólidos en líquidos. Consiste en hacer girar la mezcla a una gran velocidad; de esta manera, las partículas más pesadas tienden a “escaparse” de la mezcla, separándose de las restantes. Lógicamente, cuanto mayor sea la masa, con mayor fuerza se separarán las partículas, que quedarán retenidas en el fondo del tubo. Esta técnica se utiliza en los laboratorios de análisis clínicos para separar y estudiar algunas de las sustancias (por ejemplo, los glóbulos rojos) que se encuentran en la sangre.


10.1.3. DECANTACIÓN
Sirve para separar dos o más líquidos inmiscibles entre ellos. El método se basa en las diferentes densidades de los líquidos que forman parte de la mezcla. Por ejemplo, en el caso de una mezcla de agua y aceite (ver figura a la derecha) el agua se sitúa por debajo debido a su mayor densidad; utilizando un embudo de decantación, abrimos la llave que se encuentra en la parte inferior y dejamos caer el agua; si cerramos la llave cuando vaya a caer el aceite, habremos conseguido separar ambos líquidos.
Sirve para separar una sustancia que forme parte de la mezcla y que posea propiedades magnéticas, es decir, se vea atraída por un imán. Estas sustancias suelen ser metales. Acercando un imán a la mezcla, conseguiremos separar aquellas sustancias que se vean atraídas por él. Esta técnica suele utilizarse en las industrias siderúrgicas para separar los metales del mineral del que proceden.
10.1.5. TAMIZADO
Es el método indicado para separar los componentes de una mezcla de sólidos según el tamaño de sus partículas. Utilizando el tamiz apropiado, retendremos en él el sólido cuyas partículas sean más gruesas.
10.2. SEPARACIÓN DE LOS COMPONENTES DE MEZCLAS HOMOGÉNEAS O DISOLUCIONES
10.2.1. CRISTALIZACIÓN
Sirve para separar una sustancia (habitualmente sólida) que se encuentra disuelta en un líquido. Para ello, se utiliza un recipiente muy ancho llamado cristalizador (ver figura a la derecha), en el cual se vierte la disolución; entonces, si se deja evaporar lentamente, el agua va pasando a estado gaseoso y las partículas de la sustancia sólida se unen poco a poco formando cristales con formas geométricas definidas (rombos, polígonos, etc.). Un ejemplo de cristalización es la separación de la sal del agua del mar en las salinas. La cristalización se puede acelerar aún más mediante el calentamiento a sequedad, que consiste en calentar la disolución en una cápsula de porcelana (ver figura a la izquierda) que se pone en contacto con una fuente de calor (hornillo, mechero,...). En este caso, los cristales de sólido que se obtienen al evaporarse el líquido son de menor tamaño que los que se obtienen a partir de la cristalización.


10.2.2. DESTILACIÓN
Sirve para separar una mezcla de dos o más líquidos miscibles entre sí. Para ello, se utiliza un dispositivo como el de la izquierda: se introduce la mezcla de líquidos en el matraz y comienza a calentarse. Entonces, el líquido con menor punto de ebullición comenzará a evaporarse antes que los demás; el agua corre por el tubo refrigerante enfriando dicho vapor, transformándolo en estado líquido (condensación). El líquido termina por caer en el recipiente colector, separándose así del resto de la mezcla. Para que la destilación sea eficaz, los líquidos deben tener puntos de ebullición que se diferencien en, al menos, 10 ºC.

11. DISOLUCIONES.
11.1. COMPONENTES Y FORMACIÓN.
Una disolución es una mezcla homogénea formada por dos componentes:
- Soluto: es el componente que aparece, habitualmente, en menor proporción. Suele ser el más importante. En una disolución puede haber varios solutos.
- Disolvente: es el componente que aparece en mayor proporción. Si el agua forma parte de la disolución, siempre será el disolvente (es por eso por lo que se le llama disolvente universal). Suele ser el menos importante.
SOLUTO
|
DISOLVENTE
|
DISOLUCIÓN
|
EJEMPLO
|
GAS
|
GAS
|
GAS
|
AIRE
|
LÍQUIDO
|
NIEBLA
| ||
SÓLIDO
|
POLVO EN EL AIRE
| ||
GAS
|
LÍQUIDO
|
LÍQUIDO
|
AMONIACO COMERCIAL
|
LÍQUIDO
|
ALCOHOL Y AGUA
| ||
SÓLIDO
|
SAL Y AGUA
| ||
GAS
|
SÓLIDO
|
SÓLIDO
|
HIDRÓGENO EN PALADIO
|
LÍQUIDO
|
AMALGAMAS (MERCURIO-METAL)
| ||
SÓLIDO
|
ACERO INOXIDABLE
|
El soluto y el disolvente pueden encontrarse en cualquiera de los 3 estados de agregación; en la tabla que aparece a continuación aparecen algunos ejemplos de disoluciones tomados de la vida cotidiana en los que el soluto y el disolvente aparecen en distintos estados de agregación. Esta tabla nos da una idea de la importancia de las disoluciones, pues multitud de sustancias naturales y artificiales se presentan de este modo; incluso casi todos los procesos biológicos que tienen lugar en el interior de los organismos vivos suceden entre sustancias disueltas en agua.
Hemos dicho al principio del apartado 1 que una disolución o mezcla homogénea tiene la misma composición y propiedades en todos sus puntos, es decir, que sus componentes no pueden distinguirse a simple vista. Podemos explicar esto a partir de la teoría cinético-molecular, aplicándolo al ejemplo de una disolución de sal (o cloruro de sodio) en agua: cuando se disuelve la sal en agua, los granos de sal son atraídos por las moléculas de agua, de modo que cada grano de sal se va fragmentando (o rompiendo) en partículas de cloro y de sodio, que son muy pequeñas e invisibles a simple vista. Ésta es la razón de que no podamos distinguir a simple vista los componentes de una disolución.
El volumen resultante de la mezcla entre el soluto y el disolvente no es aditivo, pues debido al reajuste de espacios entre las distintas partículas del soluto y del disolvente, el volumen final es inferior al de la suma de ellos (aunque en los ejercicios consideraremos que los volúmenes sí son aditivos). Sin embargo, la masa de la disolución resultante sí es aditiva, es decir, es igual a la suma de las masas de soluto y disolvente.
Disolvente
|
Soluto
|
Disolución
| |
Gas
|
Gas
|
Aire
| |
Líquido
|
Niebla
| ||
Sólido
|
Humo
| ||
Líquido
|
Gas
|
Refrescos con gas (coca-cola)
| |
Líquido
|
Gasolina
| ||
Sólido
|
Agua del mar
| ||
Sólido
|
Gas
|
Gases absorbidos por carbono activo
| |
Líquido
|
Amalgamas
| ||
Sólido
|
Aleaciones (acero = hierro y carbono)
| ||
11.2.1. CONCEPTO
No todas las sustancias se disuelven con la misma facilidad en un disolvente (por ejemplo, agua). A la cantidad máxima de soluto que puede disolverse en una cierta cantidad de disolvente a una cierta temperatura se le llama solubilidad de la sustancia. Así pues, la solubilidad de las sustancias depende de la temperatura y del estado de agregación en que se encuentre el soluto; así, tenemos:
- Si el soluto es sólido o líquido, su solubilidad aumenta si aumenta la temperatura, es decir, se disolverá más cantidad de soluto si aumenta la temperatura de la disolución. Así, por ejemplo, es más fá - cil disolver el colacao en leche caliente que en leche fría.
- Si el soluto es gaseoso, su solubilidad aumenta si disminuye la temperatura, es decir, se disolverá más cantidad de soluto si disminuye la temperatura de la disolución. Es lo que sucede, por ejemplo, con la cocacola: si se abre una botella se escucha salir menor cantidad de gas cuando ésta se encuentra en la nevera.
A partir del concepto de solubilidad, podemos clasificar las disoluciones en varios tipos:
- Diluidas: son aquellas disoluciones que tienen una cantidad de soluto disuelta muy inferior a la solubilidad de dicho soluto. Lógicamente, para diluir una disolución deberemos añadirle mayor cantidad de disolvente (a este proceso se le llama dilución).
- Concentradas: son aquellas disoluciones que tienen una cantidad de soluto muy próxima al valor de la solubilidad de dicho soluto. Para hacer una disolución más concentrada deberemos añadirle más soluto.
- Saturadas: son aquellas disoluciones que tienen, a una cierta temperatura, la cantidad máxima posible de soluto que pueda estar disuelta.
- Sobresaturadas: son aquellas disoluciones que, tras previo cambio en la temperatura, pueden admitir una cantidad de soluto mayor que su solubilidad. Si, por ejemplo, el soluto es sólido, podrá disolverse una cantidad mayor de soluto si aumentamos la temperatura de la disolución.
11.2.3. CURVAS DE SOLUBILIDAD
Las curvas de solubilidad son representaciones gráficas que nos permiten estudiar cómo varía la solubilidad de una sustancia en agua, ya sea dicha sustancia sólida, líquida o gaseosa, conforme varía (aumenta o disminuye) su temperatura. En el eje horizontal aparecen las temperaturas en ºC, y en el eje vertical aparece la solubilidad de la sustancia expresada generalmente en g de sustancia/100 g de agua (ó g de sustancia/100 ml de agua).
| Temperatura | 20 ºC | 30 ºC | 40 ºC | 50 ºC | 60 ºC |
| Masa disuelta en 100 g de agua | 30 | 44 | 60 | 80 | 104 |
PRÁCTICA

11.3. CONCENTRACIÓN DE UNA DISOLUCIÓN.
11.3.1. CONCEPTO
La concentración de una disolución es una magnitud que nos indica la relación entre la cantidad de soluto que hay disuelta en una cierta cantidad de disolvente o de disolución. Así pues, la concentración nos indica cuál es la proporción entre soluto y disolvente o disolución. Obviamente, cuanto mayor sea su valor, más concentrada será la disolución; cuanto más pequeña sea la concentración, más diluida será. Ahora bien, el soluto que se disuelve se reparte por igual en toda la disolución, lo cual significa que la proporción entre soluto y disolvente no depende de la cantidad de disolución que se examine. Un ejemplo de lo dicho sucede si disolvemos dos cucharadas de azúcar en un vaso de leche: la leche estará igual de dulce si nos tomamos medio vaso, una cucharada o el vaso entero.
11.3.2. FORMAS DE EXPRESAR LA CONCENTRACIÓN
Existen muchas formas de expresar la concentración de una disolución. Este curso veremos sola - mente 3 de ellas: el porcentaje en masa, el porcentaje en volumen y la concentración expresada en g/l.
11.3.2.1. PORCENTAJE EN MASA
El porcentaje en masa de una disolución nos indica la relación entre la masa de soluto y la masa de disolución en que está disuelta. Se calcula de la siguiente manera:
% en masa =
masa soluto / masa disolución · 100
Ejemplo: Preparamos una disolución que contiene 2 g de cloruro de sodio (NaCl) y 3 g de cloruro de potasio (KCl) en 100 g de agua destilada. Calcula el tanto por ciento en masa de cada soluto en la disolución obtenida.
Primeramente, se trata de identificar a los solutos y al disolvente. En este caso, el disolvente es el agua, pues es la sustancia que se encuentra en mayor proporción y los solutos serán NaCl y KCl. La masa de soluto será la que hay para cada uno de ellos; la masa de disolución es la suma de todas las masas de sustancias presentes en la mezcla: 2 g + 3 g + 100 g = 105 g. Por tanto:
% en masa de NaCl = (2 g / 105 g) · 100 = 1,9 % de NaCl en la disolución.
% en masa de KCl = (3 g / 105 g) · 100 = 2,8 % de KCl en la disolución.
Esto indica que si tuviésemos 100 g de disolución, 1,9 g serían de cloruro sódico, 2,8 g serían de cloruro potásico y el resto, hasta 100 g, serían de agua.
11.3.2.2. PORCENTAJE EN VOLUMEN
El porcentaje en volumen de una disolución relaciona el volumen de soluto con el volumen de disolución en que éste está disuelto. Se calcula de la siguiente manera:
% en volumen =
volumen soluto / volumen disolución · 100
Ejemplo: Preparamos una disolución añadiendo 5 ml de alcohol etílico junto a 245 ml de agua. Calcula el % en volumen de soluto en la disolución.
En este caso, el soluto es el alcohol pues está en menor cantidad y el disolvente es el agua. El volumen de disolución es la suma de volúmenes de los componentes (no tiene porqué ser así siempre): 5 ml + 245 ml = 250 ml. Por tanto:
% en volumen de alcohol = (5 ml / 250 ml) · 100 = 2 % de alcohol en la disolución.
11.3.2.3. CONCENTRACIÓN EN g/L
La concentración expresada en g/l de una disolución (abreviadamente la representaremos con la letra C) se define como la masa de soluto, expresada en gramos, que hay disuelta en el volumen de disolución, expresado en litros, en que está disuelto. Se calcula de la siguiente manera:
C =
g soluto / V(L) disolución
Ejemplo: Preparamos una disolución añadiendo 20 g de sal a agua destilada hasta tener un volumen de 500 ml. Calcular la concentración en masa.
En este caso, el soluto es la sal y el disolvente es el agua. El volumen de disolución es 500 ml = 0,5 litros. Por tanto:
Concentración en masa = 20 g / 0,5 l = 40 g/l.
En este caso, el soluto es la sal y el disolvente es el agua. El volumen de disolución es 500 ml = 0,5 litros. Por tanto:
Concentración en masa = 20 g / 0,5 l = 40 g/l.
12. CUESTIONES




Estado sólido
Estado líquido
Cuestiones (I)
Cuestiones (II)
Ejercicios de cálculo de densidades
Sustancias puras
Clasificación de la materia
Sustancias puras
Mexclas
Métodos de separación
Estados de la materia
Clasificación materia
Distinguir sustancias
Disoluciones
Concentración de disoluciones
Medida de la solubilidad
Variación de la solubilidad
Separación de mezclas
Preparación de disoluciones
Estados de agregación
Cálculos de masa y densidad
Estados de la materia
Ebullición
Cambios de estado
Disoluciones 2
Mezclas
Disoluciones 3
Test
Materia
13. PRÁCTICAS
Estudio del estado sólido
Estudio del estado líquido
Gas a temperatura constante
Gas a presión constante
Gas a volumen constante
Introducción
Fusión
Evaporación
Ebullición
Sublimación
Visión global


Ejercicio de solubilidad







La Materia. Propiedades y características
Clasificación de la materia: Mezclas y sustancias puras. Separación de mezclas I
Clasificación de la materia:Mezclas y sustancias puras. Separación de mezclas II
15. VÍDEOS
Vídeo 1
Vídeo 2
Vídeo 3
Vídeo 4




Estado sólido
Estado líquido
Cuestiones (I)
Cuestiones (II)
Ejercicios de cálculo de densidades
Sustancias puras
Clasificación de la materia
Sustancias puras
Mexclas
Métodos de separación
Estados de la materia
Clasificación materia
Distinguir sustancias
Disoluciones
Concentración de disoluciones
Medida de la solubilidad
Variación de la solubilidad
Separación de mezclas
Preparación de disoluciones
Estados de agregación
Cálculos de masa y densidad
Estados de la materia
Ebullición
Cambios de estado
Disoluciones 2
Mezclas
Disoluciones 3
Test
13. PRÁCTICAS
Estudio del estado sólido
Estudio del estado líquido
Gas a temperatura constante
Gas a presión constante
Gas a volumen constante
Introducción
Fusión
Evaporación
Ebullición
Sublimación
Visión global


Ejercicio de solubilidad








14. OTROS CONTENIDOS
Materia: Definición, propiedades no características. Unidades de medidasLa Materia. Propiedades y características
Clasificación de la materia: Mezclas y sustancias puras. Separación de mezclas I
Clasificación de la materia:Mezclas y sustancias puras. Separación de mezclas II
15. VÍDEOS
Vídeo 1
Vídeo 2
Vídeo 3
Vídeo 4













No hay comentarios:
Publicar un comentario