ÍNDICE
|
8. Reacciones de óxido reducción 9. Reacciones ácido base 10. Desplazamiento electrónico 11. Reacciones de los alcanos 12. Reacciones de ,los alquenos 13. Reacciones de los alquinos 14. Reacciones del benceno 15. Polímeros de adición 16. Reacciones de los alcoholes 17. Reacciones de los aldehidos y cetonas 18. Reacciones de los ácidos carboxílicos 19. Reacciones de los ésteres 20. Reacciones de las aminas 21. Reacciones de las amidas 22. Reacciones de los nitrilos 23. Cuestiones 24. Prácticas 25. Vídeos |
1. ESQUEMAS
2. PRESENTACIONES









3. ISOMERÍA
Dos compuestos son isómeros cuando sus moléculas están formadas por el mismo número y clase de átomos, pero agrupados de distinta forma, de modo que sus propiedades físico-químicas son totalmente distintas. Tendrán la misma fórmula molecular, pero distinta fórmula estructural.
Son isómeros el gliceraldehído, la dihidroxiacetona y el ácido láctico porque son tres compuestos distintos con la misma fórmula molecular C3H6O3.
Los diversos tipos de isomería se pueden clasificar atendiendo a los conceptos de


Etanol Dimetileter
Hay varios tipos de isomería:

3.1. Isómeros estructurales:
Isómeros de cadena: estos isómeros se presentan en compuestos que difieren en la posición de los átomos en la cadena carbonada. Estos isómeros son característicos de los alcanos y cicloalcanos.
Los diversos tipos de isomería se pueden clasificar atendiendo a los conceptos de
- Constitución: Distinta ordenación o naturaleza de los enlaces
- Configuración: Disposición tridimensional de los átomos de una molécula en el espacio, sin considerar los casos debidos a la rotación de grupos en torno a enlaces sencillos C2H6O
Etanol Dimetileter
Hay varios tipos de isomería:
3.1. Isómeros estructurales:
Isómeros de cadena: estos isómeros se presentan en compuestos que difieren en la posición de los átomos en la cadena carbonada. Estos isómeros son característicos de los alcanos y cicloalcanos.
3.1.1. Isomería de cadena u ordenación
Presentan isomería de cadena u ordenación aquellos compuestos que tienen distribuidos los átomos de C de la molécula de forma diferente.


En la siguiente figura se observan isómeros de alcanos cíclicos: C8H16



3.1.2. Isómeros de posición
En la siguiente figura se observan isómeros de alcanos cíclicos: C8H16
3.1.2. Isómeros de posición
Estos compuestos presentan la misma cadena o anillo y los mismos grupos funcionales, pero difieren en la posición o posiciones a las cuales están unidos esos grupos, por lo que las propiedades físicas e incluso las químicas varían.




3.1.3. Isómeros de función
3.1.3. Isómeros de función
Estos isómeros se distinguen por presentar grupos funcionales diferentes. Los isómeros se presentan entre compuestos diferentes tales como:
- dienos y alquinos
- aquenos y cicloalcanos
- aldehídos y cetonas, alcoholes
- éteres, ácidos
- ésteres, entre otros.
(1-propanol) (metoxietano)
3.2. Conformaciones espaciales:
Incluso tras establecer la configuración de cada uno de los carbonos, la disposición de la molécula en el espacio no queda completamente especificada. En efecto, las moléculas cuyos átomos están unidos por enlaces sencillos son susceptibles de adoptar varias posiciones espaciales interconvertibles por rotación en torno a un enlace sencillo.
Estas disposiciones se conocen como conformaciones espaciales
Para distinguir las conformaciones espaciales es útil recurrir a la llamada proyección de Newman que intercala un disco imaginario entre los dos carbonos, de manera que las valencias próximas al espectador se ven enteras, mientras que las más alejadas sólo se ven en la parte que sobresale del disco. En la Figura se representa una visón lateral (representación en caballete) y las proyecciones de Newman que resultan al observar la molécula desde cada extremo.
Así, en la rotación de los dos grupos metilo que constituyen el etano (CH3-CH3) se pueden distinguir dos conformaciones extremas, que se llaman eclipsada y alternada, según la posición relativa de los hidrógenos enlazantes
En el caso frecuente de que los sustituyentes de cada carbono sean distintos, las posibilidades de presentar conformaciones distintas se multiplican. Las formas más estables, por lo general, son las que tienen los sustituyentes más voluminosos en posiciones alternadas anti. Asi, en el caso del butano existen las siguientes conformaciones:
Eclipsada anti (sinperiplanar)
|
Alternada gauche (sinclinal)
|
Eclipsada gauche (anticlinal)
|
Alternada anti (antiperiplanar)
|
Eclipsada gauche (anticlinal)
|
Alternada gauche (sinclinal)
|
El prefijo anti se emplea cuando los enlaces de los grupos más voluminosos (en este caso los dos grupos metilo) forman angulos superiores a 90°. El prefijo sin se emplea cuando los enlaces de los grupos más voluminosos (en este caso los dos grupos metilo) forman angulos inferiores a 90°. Cuando los grupos más voluminosos están en disposición alternada formando entre sí un ángulo de 60º o de 300º se dice que están en conformación gauche.
La terminación periplanar se aplica cuando los dos grupos más voluminosos están en un mismo plano. La terminación clinal se aplica cuando los dos grupos voluminosos están en distintos planos.
Así, las cadenas hidrocarbonadas de los ácidos grasos saturados adoptan la conformación todo-anti, que es la más estable
La posibilidad de libre rotación del enlace sencillo está impedida en los hidrocarburos cíclicos. Este impedimento es prácticamente absoluto en los ciclos pequeños, de 3 o 4 átomos de carbono. En los anillos aromáticos, estabilizados por resonancia, tampoco hay posibilidad de rotación.
Sin embargo, en los anillos de 5 o más átomos de carbono, esta posibilidad de rotación no está totalmente impedida. Cada una de las conformaciones representa estados de mínima energía para la molécula, que en realidad está transformándose continuamente de una en otra.
Así, en el caso del ciclohexano, la posibilidad de rotación permite a la molécula adoptar conformaciones distintas de la plana. En cada una de estas conformaciones, la tensión del anillo es nula porque los ángulos entre los enlaces carbono-carbono son iguales a los de las valencias del carbono tetraédrico y porque todos los carbonos, considerados dos a dos, adoptan preferentemente conformación alternada. En la conformación bote, las parejas de carbonos 2-3 y 5-6 son eclipsadas (bolas rojas en la figura inferior) y las restantes son alternadas-sin. En la conformación silla todas las parejas posibles son alternadas-sin, y por tanto es más estable. (Lo puedes comprobar rotando cada una de las moléculas de la tabla inferior).
3.4. Estereoquímica
La estereoquímica es el estudio de los compuestos orgánicos en el espacio. Para comprender las propiedades de los compuestos orgánicos es necesario considerar las tres dimensiones espaciales.

Las bases de la estereoquímica fueron puestas por Jacobus van’t Hoff y Le Bel, en el año 1874. De forma independiente propusieron que los cuatro sustituyentes de un carbono se dirigen hacia los vértices de un tetraedro, con el carbono en el centro del mismo.
La disposición tetraédrica de los sustituyentes de un carbono sp3 da lugar a la existencia de dos posibles compuestos, que son imágenes especulares no superponibles, llamados enantiómeros.
En general a las moléculas que se diferencian por la disposición espacial de sus átomos, se les denomina estereoisómeros.
Los isómeros son moléculas que tienen la misma fórmula molecular pero diferente estructura. Se clasifican en isómeros estructurales y estereoisómeros. Los isómeros estructurales difieren en la forma de unión de sus átomos y se clasifican en isómeros de cadena, posición y función.
3.4.1. Isómeros geométricos
En un compuesto orgánico la rotación alrededor de un enlace simple carbono-carbono es libre, esto permite que los átomos de dicho compuesto tomen posiciones relativas formando las denominadas conformaciones.
La diferencia energética para alcanzar una configuración u otra es muy pequeña apenas de 6 a 6 Kcal/mol, esto hace imposible asilar las diferentes conformaciones de los compuestos que presentan enlaces simples.
Cuando se trata de compuestos con doble enlace carbono-carbono, la rotación está restringida por la cantidad de energía. El doble enlace es rígido y sólo puede producirse si el doble enlace se rompe, para lo cual es necesario alrededor de 70 Kcal/mol.
Diasterómeros
Son estereoisómeros que no se relacionan como objeto e imagen epecular. Son relativamente fáciles de distinguir ya que sus propiedades físicas (punto de fusión, solubilidad, propiedades cromatográficas...) y químicas (reactividad) suele ser diferentes.
Los isómeros cis-trans tienen la misma cadena con las mismas funciones en las mismas posiciones, pero debido a que la molécula es rígida, cabe la posibilidad de que dos grupos funcionales estén más próximos en el espacio (cis) o más alejados (trans). La rigidez de la molécula se debe normalmente a la presencia de:
En el caso de un doble enlace, los sustituyentes más voluminosos pueden quedar del mismo lado del doble enlace y estar más próximos en el espacio (isómero cis) o en distintos lados del doble enlace, más alejados (isómero trans).Veamos un ejemplo:


Configuración CIS: esta configuración se presenta cuando grupos idénticos (hidrógenos, halógenos, etc.) aparecen en un mismo lado del plano

 Configuración TRANS: esta configuración se presenta cuando los dos grupos idénticos aparecen en lados opuestos de ese plano.
Configuración TRANS: esta configuración se presenta cuando los dos grupos idénticos aparecen en lados opuestos de ese plano.


Cuando existen varios sustituyentes distintos, la nomenclatura cis-trans puede resultar ambigua. En estos casos se adopta la nomenclatura E-Z
En consecuencia:
 Los isómeros geométricos de una sustancia determinada pueden ser separados experimentalmente, debido a que su configuración les otorga propiedades físicas que los diferencian. Es así que los isómeros Cis son más polares, presentan punto de ebullición más altos y punto de fusión más bajo.
Los isómeros geométricos de una sustancia determinada pueden ser separados experimentalmente, debido a que su configuración les otorga propiedades físicas que los diferencian. Es así que los isómeros Cis son más polares, presentan punto de ebullición más altos y punto de fusión más bajo.
3.5. Isómeros Ópticos
La diferencia energética para alcanzar una configuración u otra es muy pequeña apenas de 6 a 6 Kcal/mol, esto hace imposible asilar las diferentes conformaciones de los compuestos que presentan enlaces simples.
Cuando se trata de compuestos con doble enlace carbono-carbono, la rotación está restringida por la cantidad de energía. El doble enlace es rígido y sólo puede producirse si el doble enlace se rompe, para lo cual es necesario alrededor de 70 Kcal/mol.
Diasterómeros
Son estereoisómeros que no se relacionan como objeto e imagen epecular. Son relativamente fáciles de distinguir ya que sus propiedades físicas (punto de fusión, solubilidad, propiedades cromatográficas...) y químicas (reactividad) suele ser diferentes.
Los isómeros cis-trans tienen la misma cadena con las mismas funciones en las mismas posiciones, pero debido a que la molécula es rígida, cabe la posibilidad de que dos grupos funcionales estén más próximos en el espacio (cis) o más alejados (trans). La rigidez de la molécula se debe normalmente a la presencia de:
- un doble enlace
- un anillo
En el caso de un doble enlace, los sustituyentes más voluminosos pueden quedar del mismo lado del doble enlace y estar más próximos en el espacio (isómero cis) o en distintos lados del doble enlace, más alejados (isómero trans).Veamos un ejemplo:
En consecuencia:
- el isómero Z (zusammen) será el que tenga los dos sustituyentes de mayor jerarquía (a los que se ha asignado el número 1) del mismo lado del doble enlace (más próximos en el espacio)
- el isómero E (entgegen) será el que los tenga los dos sustituyentes de mayor jerarquía a distinto lado del doble enlace (más separados en el espacio)
3.5. Isómeros Ópticos
La actividad óptica es la capacidad de una sustancia quiral para rotar el plano de la luz polarizada. Se mide usando un aparato llamado polarímetro.
¿Qué es luz polarizada?
La luz normal consiste en ondas electromagnéticas que vibran en todas las direcciones. Cuando la luz pasa a través de un polarizador (prisma de Nicol) las ondas electromagnéticas vibran en un plano. Este plano de oscilación coincide con el plano de propagación de la onda.
Cuando la luz polarizada pasa a través de una cubeta que contiene una sustancia quiral, se produce una rotación en el plano de polarización.
Las sustancias quirales rotan la luz polarizada y se dice de ellas que son ópticamente activas (presentan actividad óptica). Aquellas sustancias que no producen rotación en la luz polarizada son ópticamente inactivas.
Los isómeros ópticos son sustancias que física y químicamente son iguales, su diferencia se encuentra en que desvían un rayo de luz polarizada en distinto sentido. Si la desvían en el sentido de las agujas del reloj (hacia la derecha) se denomina compuesto dextrógiro y se representa con el signo (+), si lo hacen en sentido contrario (hacia la izquierda) se denomina compuesto levógiro (-).
La luz sin polarizar vibra en muchas direcciones que se resuelven en planos perpendiculares entre si.
Cuando la luz polarizada pasa a través de una cubeta que contiene una sustancia quiral, se produce una rotación en el plano de polarización.
Las sustancias quirales rotan la luz polarizada y se dice de ellas que son ópticamente activas (presentan actividad óptica). Aquellas sustancias que no producen rotación en la luz polarizada son ópticamente inactivas.
Cuando un compuesto ópticamente activo, rota la luz polarizada en el sentido de las agujas del reloj, se dice que es dextrógiro y se representa por (+). Las sustancias que rotan la luz en sentido contrario a las agujas del reloj, son levógiras levógiras y se representa por (-).
 Los enantiómeros rotan la luz polarizada el mismo ángulo pero en sentidos opuestos. Mediante un polarímetro puede medirse dicho ángulo.
Los enantiómeros rotan la luz polarizada el mismo ángulo pero en sentidos opuestos. Mediante un polarímetro puede medirse dicho ángulo.
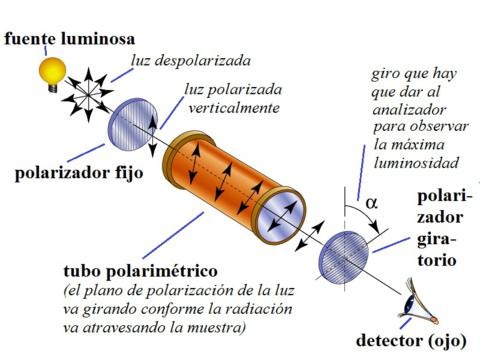

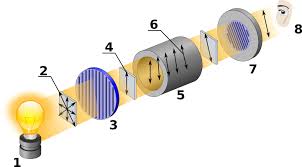
Para polarizar la luz se usa un prisma de Nicol que consiste en dos cristales de calcita (CaCO3) unidos por bálsamo de Canadá. Cuando la luz atraviesa el prisma se divide en dos rayos: uno ordinario que vibra en el plano del papel y que es reflejado totalmente por la capa del bálsamo de Canadá y otro extraordinario que emerge del prisma y vibra en planos paralelos (en un solo plano). Este último es el rayo de luz polarizada y es el que se hace incidir sobre la sustancia cuya desviación óptica se quiere medir y para lo cual se utiliza el polarímetro.
El polarímetro consta de dos prismas de Nicol, uno llamado polarizador y el otro llamado analizador, éste último puede ser girado y presenta una escala graduada que permite medir en grados el signo y la amplitud de la desviación que experimenta el rayo de luz polarizada. El número de grados el signo y la amplitud de la desviación que experimenta el rayo de luz polarizada. El número de grados de la rotación depende de la naturaleza de la sustancia disuelta, de la distancia (longitud del recorrido) que recorre la luz a través de la solución y de la concentración de la solución.
El poder óptico rotatorio de una sustancia viene dado por la falta de simetría de sus moléculas debido, generalmente, a la existencia de un carbono asimétrico.



Un carbono asimétrico es aquel que está unido a cuatro sustituyentes diferentes.
Un isómero óptico es la imagen especular del otro (imagen opuesta tipo espejo), ambos reciben el nombre de enantiómeros, enantiomorfos o antípodas ópticas.
¿Qué es luz polarizada?
La luz normal consiste en ondas electromagnéticas que vibran en todas las direcciones. Cuando la luz pasa a través de un polarizador (prisma de Nicol) las ondas electromagnéticas vibran en un plano. Este plano de oscilación coincide con el plano de propagación de la onda.
Cuando la luz polarizada pasa a través de una cubeta que contiene una sustancia quiral, se produce una rotación en el plano de polarización.
Las sustancias quirales rotan la luz polarizada y se dice de ellas que son ópticamente activas (presentan actividad óptica). Aquellas sustancias que no producen rotación en la luz polarizada son ópticamente inactivas.
Los isómeros ópticos son sustancias que física y químicamente son iguales, su diferencia se encuentra en que desvían un rayo de luz polarizada en distinto sentido. Si la desvían en el sentido de las agujas del reloj (hacia la derecha) se denomina compuesto dextrógiro y se representa con el signo (+), si lo hacen en sentido contrario (hacia la izquierda) se denomina compuesto levógiro (-).
La luz sin polarizar vibra en muchas direcciones que se resuelven en planos perpendiculares entre si.
Cuando la luz polarizada pasa a través de una cubeta que contiene una sustancia quiral, se produce una rotación en el plano de polarización.
Las sustancias quirales rotan la luz polarizada y se dice de ellas que son ópticamente activas (presentan actividad óptica). Aquellas sustancias que no producen rotación en la luz polarizada son ópticamente inactivas.
Cuando un compuesto ópticamente activo, rota la luz polarizada en el sentido de las agujas del reloj, se dice que es dextrógiro y se representa por (+). Las sustancias que rotan la luz en sentido contrario a las agujas del reloj, son levógiras levógiras y se representa por (-).


Para polarizar la luz se usa un prisma de Nicol que consiste en dos cristales de calcita (CaCO3) unidos por bálsamo de Canadá. Cuando la luz atraviesa el prisma se divide en dos rayos: uno ordinario que vibra en el plano del papel y que es reflejado totalmente por la capa del bálsamo de Canadá y otro extraordinario que emerge del prisma y vibra en planos paralelos (en un solo plano). Este último es el rayo de luz polarizada y es el que se hace incidir sobre la sustancia cuya desviación óptica se quiere medir y para lo cual se utiliza el polarímetro.
El polarímetro consta de dos prismas de Nicol, uno llamado polarizador y el otro llamado analizador, éste último puede ser girado y presenta una escala graduada que permite medir en grados el signo y la amplitud de la desviación que experimenta el rayo de luz polarizada. El número de grados el signo y la amplitud de la desviación que experimenta el rayo de luz polarizada. El número de grados de la rotación depende de la naturaleza de la sustancia disuelta, de la distancia (longitud del recorrido) que recorre la luz a través de la solución y de la concentración de la solución.
El poder óptico rotatorio de una sustancia viene dado por la falta de simetría de sus moléculas debido, generalmente, a la existencia de un carbono asimétrico.

Un isómero óptico es la imagen especular del otro (imagen opuesta tipo espejo), ambos reciben el nombre de enantiómeros, enantiomorfos o antípodas ópticas.

3.6. La nomenclatura D-L
Los enantiomorfos presentan las mismas propiedades químicas y físicas (excepto su acción sobre la luz polarizada). Una mezcla equimolecular (igual número de moléculas) de dos enantiomorfos no presentará actividad óptica. A esta mezcla se le llama mezcla racémica.
El caso más frecuente de ausencia de plano de simetría se debe a que algún carbono tetraédrico está unido a cuatro radicales distintos. Este carbono recibe el nombre de carbono asimétrico (Figura de la derecha). Para representar en un plano los carbonos asimétricos se han ideado varias representaciones convencionales en proyección. La más utilizada es la de Fischer (Figura de la derecha). Según esta convención, se proyecta la molécula sobre el plano del papel con las siguientes condiciones:
- La cadena carbonada se sitúa en vertical, con las valencias que la integran en dirección a la parte posterior del plano.
- La cadena se orienta con la parte más oxidada hacia arriba y la más reducida hacia abajo.
- Las valencias que no integran la cadena carbonada resultan horizontales y dirigidas hacia la parte anterior del plano
En los azúcares se considera grupo funcional al grupo OH del penúltimo carbono (por ser el carbono asimétrico más alejado del grupo aldehído o cetona)
en los aminoácidos se considera grupo funcional al grupo amino (NH2) del segundo carbono (carbono a)
D-gliceraldehído (3D)
|
D-gliceraldehído (Proyección de Fischer)
|
L-gliceraldehído (Proyección de Fischer)
| |
L-aminoácido (3D)
|
D-aminoácido (Proyección de Fischer)
|
L-aminoácido (Proyección de Fischer)
| |
La nomenclatura D-L no indica si el compuesto es dextrógiro o levógiro. En el caso del gliceraldehído, el isómero D es dextrógiro, y se indica con el signo (+), pero no siempre tiene por qué ser así.
La nomenclatura D-L es inequívoca para designar la configuración de isómeros con un solo carbono asimétrico. Sin embargo, cuando en una molécula hay varios centros de asimetría es más conveniente utilizar el sistema propuesto por Cahn, Ingold y Prelog.
3.7. Configuración absoluta R-S
La nomenclatura D-L es inequívoca para designar la configuración de isómeros con un solo carbono asimétrico. Sin embargo, cuando en una molécula hay varios centros de asimetría es más conveniente utilizar el sistema propuesto por Cahn, Ingold y Prelog (foto de la izquierda), que permite establecer la configuración absoluta de cada átomo. Con esta nomenclatura se puede asignar un nombre sistemático y discriminativo a moléculas isoméricas complejas.
Así, se podrán distinguir y nombrar diferentes isómeros con varios carbonos asimétricos. Según esta convención, las dos configuraciones posibles de cada carbono asimétrico se designarían con las letras R y S (nomenclatura R-S). En algunos casos, R coincidirá con D, pero en otros no.
Para determinar la configuración de un carbono hay que seguir ciertas reglas. Al igual que en el caso de la isomería geométrica (nomenclatura E-Z), se jerarquizan los cuatro sustituyentes del carbono asimétrico usando el mismo criterio (número atómico decreciente):
Para determinar la configuración de un carbono hay que seguir ciertas reglas. Al igual que en el caso de la isomería geométrica (nomenclatura E-Z), se jerarquizan los cuatro sustituyentes del carbono asimétrico usando el mismo criterio (número atómico decreciente):
- Se ordenan los cuatro grupos sustituyentes del carbono asimétrico por orden decreciente de número atómico de los átomos enlazados directamente con dicho carbono.
- Si dos o más de estos átomos son iguales se recurre a considerar los átomos unidos a ellos con el mismo criterio de preferencia.
- Si la ambigüedad persiste, se atiende al tipo de enlace que une los átomos en cuestión y se da preferencia al enlace triple sobre el doble y al doble sobre el sencillo.
- hacia la derecha (en sentido horario). En este caso se tratará del isómero R (rectum = derecha)
- hacia la izquierda (sentido antihorario). En este caso se tratará del isómero S (sinister = izquierda)
(R)-1-bromo-1-cloro-1-fluorometano
|
(S)-1-bromo-1-cloro-1-fluorometano
| ||
Cuando hay más de un carbono asimétrico (como en la mayoría de los azúcares) aumentan las posibilidades de isomería. El número de isómeros posibles es 2n (siendo n el número de carbonos asimétricos).
Resumen
ANIMACIONES



4. PROYECCIÓN DE FISHER
Proyectar consiste en dibujar en dos dimensiones (plano) una molécula. En la proyección de Fischer la molécula se dibuja en forma de cruz con los sustituyentes que van al fondo del plano en la vertical y los grupos que salen hacia nosotros en la horizontal, el punto intersección de ambas líneas representa el carbono proyectado.
 Aunque se acostumbra a dejar la cadena carbonada en la vertical, puede girarse la molécula de diferentes formas dando lugar a proyecciones de Fischer aparentemente diferentes, pero que en realidad representan la misma molécula.
Aunque se acostumbra a dejar la cadena carbonada en la vertical, puede girarse la molécula de diferentes formas dando lugar a proyecciones de Fischer aparentemente diferentes, pero que en realidad representan la misma molécula.
Para comprobar que la proyección está bien hecha, vamos a dar notación R/S a la molécula y a su proyección.
 Ahora haremos la proyección de una molécula con dos centros quirales
Ahora haremos la proyección de una molécula con dos centros quirales
 Para proyectar una molécula en Fischer es necesario dibujarla en la conformación eclipasada. Los sustituyentes que nos quedan en el plano van colocados arriba y abajo en la proyección. Los grupos que salen hacia nosotros (cuñas) se disponen a la derecha en la proyección, y los que van al fondo (lineas a trazos) se disponen a la izquierda.
Para proyectar una molécula en Fischer es necesario dibujarla en la conformación eclipasada. Los sustituyentes que nos quedan en el plano van colocados arriba y abajo en la proyección. Los grupos que salen hacia nosotros (cuñas) se disponen a la derecha en la proyección, y los que van al fondo (lineas a trazos) se disponen a la izquierda.
 Para dar notación R/S en proyecciones de Fischer se siguen las mismas reglas que para una molécula dibujada en el espacio.
Para dar notación R/S en proyecciones de Fischer se siguen las mismas reglas que para una molécula dibujada en el espacio.
 Notación R/S a una proyección de Fischer con dos centros quirales.
Notación R/S a una proyección de Fischer con dos centros quirales.
 La notación R/S puede utilizarse para dibujar una molécula en proyección de Fischer, o bien, para pasar de la proyección de Fischer a la forma espacial de la molécula.
La notación R/S puede utilizarse para dibujar una molécula en proyección de Fischer, o bien, para pasar de la proyección de Fischer a la forma espacial de la molécula.
 Para convertir proyecciones de Newman en proyecciones de Fischer se dibuja la forma espacial de la molécula, disponiéndola en conformación eclipsada para hacer la proyección de Fischer.
Para convertir proyecciones de Newman en proyecciones de Fischer se dibuja la forma espacial de la molécula, disponiéndola en conformación eclipsada para hacer la proyección de Fischer.
 Etapas a seguir:
Etapas a seguir:

En la proyección de caballete (también llamada en prespectiva) la línea de observación forma un ángulo de 45º con el enlace carbono-carbono. El carbono más proximo al observador se encuentra abajo y a la derecha. Mientras que el más alejado está arriba a la izquierda.
Para hacer la proyección de Newman nos situamos frente al carbono señalado con la flecha, este carbono se representa por un punto (rojo), de él parten tres sustituyentes orientados del siguiente modo: metilo arriba; bromo derecha; hidrógeno izquierda. En el carbono del fondo, representado por un círculo (azul), hay otros tres sustituyentes: etilo abajo; cloro izquierda; hidrógeno derecha.
 En la proyección de Newman de la conformación eclipsada se gira ligeramente el carbono del fondo (azul) para poder dibujar sus sustituyentes. En la realidad los sustituyentes del carbono rojo tapan los del azul.
En la proyección de Newman de la conformación eclipsada se gira ligeramente el carbono del fondo (azul) para poder dibujar sus sustituyentes. En la realidad los sustituyentes del carbono rojo tapan los del azul.




Los compuestos orgánicos son objetos de múltiples reacciones de las cuales se forman gran cantidad de productos absolutamente imprescindible en el mundo actual, tales como medicinas, plásticos, detergentes, colorantes, insecticidas… Su reactividad se debe a fundamentalmente a la presencia de los grupos funcionales y puede ser debida a:

7.5.2. Reacciones nucleofílicas

y para las bases:
de las dos tablas anteriores se puede observar fácilmente que a medida que un ácido es más fuerte, su base conjugada será más débil y viceversa, si un ácido es muy débil, su base conjugada será muy fuerte.
La teoría de Brönsted ‑ Lowry también tiene sus limitaciones, ya que hay sustancias con un comportamiento típicamente ácido y que no poseen átomos de hidrógeno.
10. DESPLAZAMIENTOS ELECTRÓNICOS
10.1. Efecto inductivo:
Es un desplazamiento parcial del par electrónico de un enlace sencillo “s” hacia el átomo más electronegativo provocando fracciones de carga.
A pesar del que el hidrógeno aporta levemente al carbono su par electrónico, por convenio, se toma como punto de referencia (no provoca efecto inductivo). Así, podemos clasificar los grupos en dos tipos:
10.2. Efecto mesómero o resonancia:Es un desplazamiento del par de electrones “p” del doble enlace hacia uno de los átomos por la presencia de pares electrónicos cercanos.
Se produce cuando hay enlace múltiples y la posibilidad de que los e– se deslocalicen (átomo electronegativo con posibilidad de tener parejas de e– sin compartir). A mayor número de formas resonantes mayor estabilidad.
Ejemplo: CH2=CH–CH=CH2
Proyectar consiste en dibujar en dos dimensiones (plano) una molécula. En la proyección de Fischer la molécula se dibuja en forma de cruz con los sustituyentes que van al fondo del plano en la vertical y los grupos que salen hacia nosotros en la horizontal, el punto intersección de ambas líneas representa el carbono proyectado.

Para comprobar que la proyección está bien hecha, vamos a dar notación R/S a la molécula y a su proyección.



- Se dan prioridades por números atómicos a los sustituyentes que parten del carbono asimétrico.
- Se gira comenzando por el grupo de prioridad (a) hacia (b) y (c). Si el grupo (d) se encuentra en la vertical, el giro en el sentido de las agujas da notación R y en sentido contrario a las agujas S.





- Paso de Newman a forma espacial de la molécula.
- Giro para disponer la molécula en conformación eclipsada
- Giro que dispone los grupos que están en el plano al fondo y los que van con cuñas y líneas a trazos hacia nosotros.
- Proyección de la molécula
En la proyección de caballete (también llamada en prespectiva) la línea de observación forma un ángulo de 45º con el enlace carbono-carbono. El carbono más proximo al observador se encuentra abajo y a la derecha. Mientras que el más alejado está arriba a la izquierda.
Para hacer la proyección de Newman nos situamos frente al carbono señalado con la flecha, este carbono se representa por un punto (rojo), de él parten tres sustituyentes orientados del siguiente modo: metilo arriba; bromo derecha; hidrógeno izquierda. En el carbono del fondo, representado por un círculo (azul), hay otros tres sustituyentes: etilo abajo; cloro izquierda; hidrógeno derecha.


5. REACCIÓN QUÍMICA
Proceso mediante el cual una o más sustancias (elementos o
compuestos) denominadas reactivos, sufren un proceso de transformación o combinación para dar lugar a una serie de sustancias (elementos o compuestos)
denominadas productos. En una reacción química se produce desprendimiento o
absorción de calor u otras formas de energía.
Las transformaciones de la materia producen cambios en unas sustancias para
obtener otras diferentes. La transformación da por resultado un cambio en la
composición, constitución y/o configuración del sustrato.
En estas transformaciones, se parte de unas sustancias en el estado inicial,
llamadas reactivos, y se obtienen otras diferentes en el estado final, llamadas
productos. Por ejemplo, cuando se quema un pedazo de carbón, las sustancias
iniciales o reactivos son el carbono y el oxígeno del aire, y entre las sustancias
finales o productos, encontramos al dióxido de carbono.
Para que la reacción química tenga lugar es necesario que las sustancias iniciales
se encuentren en condiciones favorables. Volviendo al ejemplo anterior, un pedazo
de carbón no se quemará (no producirá una reacción química) si está húmedo o si
el aire contiene poco oxígeno.
Las reacciones se representan mediante ecuaciones químicas. En una ecuación
química hay dos términos. En el primero, el de la derecha, se escriben los reactivos,
expresados mediante sus fórmulas químicas correspondientes y separados por un
signo más. A la izquierda, el segundo término, en el que aparecen los productos,
también representados por sus formulas químicas correspondientes y con signos
más entre ellos. Entre ambos términos suele ponerse una flecha que indica que se
ha producido la reacción química correspondiente.

Es necesario realizar un ajuste de la ecuación química para que el número de
átomos de cada elemento en los reactivos sea igual al que existe en los productos.
Fue Lavoissier, químico francés, quien propuso que las ecuaciones químicas deben
ajustarse. Este ajuste puede hacerse de varias maneras la más sencilla de las
cuáles es la de tanteo. Resumiendo, las ecuaciones químicas son las
representaciones simbólicas de las reacciones reales. En ellas, el número de
átomos de cada elemento es el mismo en las sustancias iniciales y en las
finales.
Las reacciones químicas pueden ser representadas mediante modelos
moleculares, dibujando los átomos como si fueran esferas y construyendo así las
moléculas de las sustancias que intervienen en una reacción. Con la utilización de
los modelos moleculares podemos entender mejor la conservación de la materia
en las reacciones químicas, puesto que el número de esferas de cada clase debe
ser el mismo en las sustancias iniciales y en las finales, es decir, en los reactivos y
en los productos.
6. REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS
Los compuestos orgánicos son objetos de múltiples reacciones de las cuales se forman gran cantidad de productos absolutamente imprescindible en el mundo actual, tales como medicinas, plásticos, detergentes, colorantes, insecticidas… Su reactividad se debe a fundamentalmente a la presencia de los grupos funcionales y puede ser debida a:
- La alta densidad electrónica (doble o triple enlace)
- La fracción de carga positiva en el átomo de carbono (enlaces C–Cl, C=O, CºN).
- Efecto inductivo.
- Efecto mesómero.
7. CLASIFICACIÓN DE LAS REACCIONES ORGÁNICAS
.En cualquier texto de química orgánica aparecen un gran número de reacciones,
que son las herramientas fundamentales del químico orgánico. Su buen uso va a
depender de la organización que se haga de este recurso. La mayoría de estas
reacciones se llevan a cabo en sitios específicos de reactividad conocida como son
los grupos funcionales, y ellos constituyen un punto de referencia que nos
permitirán organizar un esquema que nos permita recordar las reacciones
involucradas. Pero lo más importante es entender como tiene lugar la reacción y
reconocer los varios parámetros que influyen en su camino de reacción. A
continuación, se indican diferentes métodos de clasificación de las reacciones más
generales en Química Orgánica.
7.1. Clasificación por el tipo de transformación
Las reacciones orgánicas se pueden agrupar y clasificar atendiendo al tipo de
transformación que tiene lugar en el compuesto orgánico como:
7.1.1. Reacciones de adición.
Este tipo de reacciones consisten en la adición de dos especies químicas al enlace
múltiple de una molécula insaturada, tal y como se indica de forma genérica en la
siguiente ecuación química:
Este tipo de reacciones es muy común en los compuestos olefínicos y acetilénicos.
Este tipo de reacciones es muy común en los compuestos olefínicos y acetilénicos
Otros ejemplos de adiciones al doble enlace: adición de bromo, adición de HBr ,
hidrogenación.
7.1.2. Reacciones de sustitución
En las reacciones de sustitución se engloban aquellas reacciones en las que un
átomo o grupo atómico es sustituido o desplazado por otro. La ecuación general
para un proceso de sustitución es:
Ejemplos de este tipo de reacciones son las que experimentan los alcoholes con
hidrácidos o las reacciones de sustitución nucleofílica de haluros de alquilo.
7.1.3. Reacciones de eliminación
Este tipo de reacciones constituyen el proceso inverso de las reacciones de adición
y consisten en la pérdida de átomos, ó grupo de átomos de una molécula, con
formación de enlaces múltiples o anillos. La formulación general de las reacciones
de eliminación es:
Ejemplos de este tipo de reacciones de eliminación son la reacción de
deshidratación de un alcohol para formar un alqueno ó la reacción de
deshidrobromación inducida por bases.
Esta clase de reacciones consisten en un reordenamiento de los átomos de una
molécula que origina otra con estructura distinta.
Un ejemplo de este tipo de reacciones es el proceso de conversión del n-butano en
isobutano en presencia de determinados catalizadores.
7.2. Clasificación por la forma en que se rompen los enlaces
Las reacciones orgánicas se pueden clasificar atendiendo a la forma en la que se
rompen y se forman los enlaces químicos en dos grandes grupos:
7.2.1. Homolítica: Suele producirse en presencia de luz UV pues se necesita un aporte de energía elevado. El enlace covalente se rompe de manera simétrica (1 e– para cada átomo) formándose radicales libres (átomos con e– desapareados).
7.2.2. Heterolítica: El enlace se rompe de manera asimétrica (uno de los átomos se queda con los dos e– que compartían). Es la ruptura más habitual, quedando con carga negativa el elemento más electronegativo y con positiva el menos,
7.2.2. Heterolítica: El enlace se rompe de manera asimétrica (uno de los átomos se queda con los dos e– que compartían). Es la ruptura más habitual, quedando con carga negativa el elemento más electronegativo y con positiva el menos,
con lo que se forman dos tipos de iones:
7.3. Clasificación por la forma en que se forman los enlaces
Las reacciones orgánicas también se pueden clasificar atendiendo al proceso de
formación de los enlaces como:
7.3.1. Reacciones de coligación
Estas reacciones se producen cuando dos radicales libres se unen formando un
enlace covalente. Este proceso es el inverso al de homólisis. Su formulación
general es:
Reciben este nombre las reacciones en las que se enlazan un anión (o una especie
con un exceso de densidad electrónica) y un catión (o una especie con huecos
electrónicos). Este proceso es el inverso al de heterólisis. Su formulación general
es:
7.4. Clasificación por la forma en que se rompen y forman los enlaces
Atendiendo a la forma en la que se rompen y forman los enlaces las reacciones se
clasifican como:
7.4.1. Reacciones no concertadas
Son aquellas en las que la rotura y formación de enlaces se produce en etapas
separadas. En esta clase de reacciones se forman especies intermedias más o
menos estables, el proceso general se indica a continuación:
7.4.2. Reacciones concertadas
Son aquellas en las que la rotura y formación de enlaces se produce
simultáneamente, como se indica a continuación:
7.5. Clasiifcación según la naturaleza del reactivo
Una clasificación importante de las reacciones orgánicas se basa en la naturaleza
del reactivo atacante. Según la definición de Lewis, un ácido es aquella especie
capaz de aceptar electrones y una base es un dador de un par de electrones.
Los reactivos electrofílicos (o electrófilos) se definen como especies capaces de
aceptar electrones y por consiguiente son acidos de Lewis.
Los reactivos nucleofílicos o nucleófilos son reactivos dadores de electrones y
por tanto bases de Lewis.
7.5.1. Reacciones electrofílicas:
7.5.2. Reacciones nucleofílicas
8. REACCIONES DE ÓXIDO-REDUCCIÓN
La oxidación y reducción no representan un tipo nuevo de reacciones sino más bien
cambios que pueden acompañar a las reacciones de adición, sustitución y
eliminación. En química inorgánica se refieren a la pérdida o ganancia de electrones
por un átomo o ión. En los compuestos orgánicos esta transferencia de electrones
no suele ser completa y el proceso redox se produce como consecuencia de un
cambio en los enlaces covalentes entre átomos de distinta electronegatividad.
Para calcular el estado de oxidación en las moléculas orgánicas se admite que el
carbono elemental se encuentra en un estado de oxidación de cero. La formación
de un enlace entre el carbono con un átomo más electronegativo es un proceso de
oxidación y la formación de un enlace entre el carbono y un átomo menos
electronegativo es un proceso de reducción, ya que en estos cambios se produce
una disminución o un aumento de la densidad electrónica sobre el átomo de
carbono.
Por ejemplo:

Las siguientes reglas pueden ayudar en la determinación de los procesos redox
orgánicos:
- Si el número de átomos de hidrógeno enlazados a un carbono aumentan, y/o si el número de enlaces a átomos más electronegativos disminuyen, el átomo de carbono en cuestión ha sido reducido.
- Si el número de átomos de hidrógeno enlazados a un carbono disminuyen , y/o si el número de enlaces a átomos más electronegativos aumentan , el átomo de carbono en cuestión ha sido oxidado.
Estas reglas se aplican en las siguientes cuatro adiciones que implican el mismo
sustrato, ciclohexeno. Los átomos de carbono coloreados de azul han sido
reducidos, mientras que los coloreados de rojo han sido oxidados.
9. REACCIONES ÁCIDO-BASE
En 1923, de forma independiente y casi simultánea, N. Brönsted (a la izquierda) y T. M. Lowry (a la derecha) elaboraron un concepto más amplio, que puede resumirse de la siguiente manera:
En 1923, de forma independiente y casi simultánea, N. Brönsted (a la izquierda) y T. M. Lowry (a la derecha) elaboraron un concepto más amplio, que puede resumirse de la siguiente manera:
- Ácido: Sustancia que tiende a dar protones a otra.
- Base: Sustancia que tiende a aceptar protones cedidos por un ácido.
Por ejemplo:
Esta teoría plantea que cuando una sustancia pierde un protón, se está comportando como un ácido, pero una vez se ha desprendido de él, como las reacciones son de equilibrio, podría volver a cogerlo por lo que se transforma en una base, la base conjugada del ácido. De manera similar, una base acepta protones, pero una vez lo ha captado, puede desprenderse de él, transformándose en un ácido, su ácido conjugado:
el ácido1 y la base1 forman lo que se denomina un par ácido ‑ base conjugado, (al igual que el ácido2 y la base2).
Según esta definición, en la reacción:
el amoniaco es una base ya que tiende a aceptar los protones cedidos por un ácido.
Estructuralmente una sustancia es un ácido en potencia si posee átomos de hidrógeno; mientras que, una sustancia es una base en potencia si posee algún átomo con un par o más de electrones no enlazantes, en los que el protón queda unido mediante un enlace covalente coordinado o dativo.
La principal ventaja de esta teoría es que permite ordenar de mayor a menor la fuerza de los ácidos. Toda sustancia capaz de ceder protones a otra, será un ácido más fuerte que ésta. Según la citada teoría, una sustancia actuará como ácido frente a otra de menor acidez y como base frente a otra de mayor acidez, es decir, que hasta un ácido puede actuar como base; por ejemplo:
HClO4 + HNO3 à NO2ClO4 + H2O
El ácido perclórico libera un protón por lo que se comporta como ácido, mientras que el ácido nítrico aquí actúa como base ya que lo capta. Por lo tanto, una sustancia actuará como base frente a cualquier otra sustancia que sea un ácido más fuerte que él, (en este caso, el ácido perclórico es más fuerte que el ácido nítrico).
Se denominan sustancias anfóteras o anfipróticas a aquellas que pueden actuar como ácido o como base según el medio en el que se encuentren. Este es el caso del agua o del ion bisulfato entre otros:
De forma análoga a la teoría de Arrhenius, también se definen las constantes de acidez y basicidad como:
que permiten ordenarlos según su fuerza relativa respecto al agua.
A continuación te mostramos dos tablas con las constantes de acidez y basicidad de los ácidos y las bases más comunes:
Para los ácidos:
| H2O | + | HCl | à | H3O+ | + | Cl- (ac) | ||
| base1 | + | ácido2 | à | ácido1 | + | base2 | ||
| CH3COOH | + | H2O | CH3COO- (ac) | + | H3O+ | |||
| ácido1 | + | base2 | base1 | + | ácido2 | |||
ácido1 + base2  base1 + ácido2
base1 + ácido2
Según esta definición, en la reacción:
HCl + NH3 à Cl- + NH4+
Estructuralmente una sustancia es un ácido en potencia si posee átomos de hidrógeno; mientras que, una sustancia es una base en potencia si posee algún átomo con un par o más de electrones no enlazantes, en los que el protón queda unido mediante un enlace covalente coordinado o dativo.
La principal ventaja de esta teoría es que permite ordenar de mayor a menor la fuerza de los ácidos. Toda sustancia capaz de ceder protones a otra, será un ácido más fuerte que ésta. Según la citada teoría, una sustancia actuará como ácido frente a otra de menor acidez y como base frente a otra de mayor acidez, es decir, que hasta un ácido puede actuar como base; por ejemplo:
HClO4 + HNO3 à NO2ClO4 + H2O
El ácido perclórico libera un protón por lo que se comporta como ácido, mientras que el ácido nítrico aquí actúa como base ya que lo capta. Por lo tanto, una sustancia actuará como base frente a cualquier otra sustancia que sea un ácido más fuerte que él, (en este caso, el ácido perclórico es más fuerte que el ácido nítrico).
Se denominan sustancias anfóteras o anfipróticas a aquellas que pueden actuar como ácido o como base según el medio en el que se encuentren. Este es el caso del agua o del ion bisulfato entre otros:
| HSO4- + OH- | |
| HSO4- + H3O+ |
HA + H2O
| ||
B + H2O
|
que permiten ordenarlos según su fuerza relativa respecto al agua.
A continuación te mostramos dos tablas con las constantes de acidez y basicidad de los ácidos y las bases más comunes:
Para los ácidos:
| Fuerza | Ácido | Base conjugada | Ka | pKa |
ácidos
fuertes
Ka > 55,55
| HClO4 | ClO4- | - | - |
| HCl, HBr, HI | Cl-, Br-, I- | - | - | |
| HNO3 | NO3- | - | - | |
| H2SO4 | HSO4- | - | - | |
| H3O+ | H2O | 55,55 | -1,74 | |
ácidos
semifuertes
55,55 > Ka > 10-4
| HIO3 | IO3- | 1,9.10-1 | 0,72 |
| H2SO3 | HSO3- | 1,7.10-2 | 1,77 | |
| HSO4- | SO4-2 | 1,2.10-2 | 1,92 | |
| HClO2 | ClO2- | 1,0.10-2 | 2,00 | |
| H3PO4 | H2PO4- | 7,5.10-3 | 2,12 | |
| HCOOH | HCOO- | 1,8.10-4 | 3,74 | |
ácidos
débiles
10-4 > Ka > 10-10
| CH3COOH | CH3COO- | 1,8.10-5 | 4,74 |
| H2CO3 | HCO3- | 4,3.10-7 | 6,37 | |
| H2S | HS- | 9,1.10-8 | 7,04 | |
| H2PO4- | HPO4-2 | 6,2.10-8 | 7,21 | |
| NH4+ | NH3 | 5,6.10-10 | 9,25 | |
| HCN | CN- | 4,9.10-10 | 9,31 | |
ácidos
muy débiles
Ka < 10-10
| HCO3- | CO3-2 | 6,0.10-11 | 10,22 |
| HIO | IO- | 1,0.10-11 | 11,00 | |
| HPO4-2 | PO4-3 | 4,8.10-13 | 12,32 | |
| HS- | S-2 | 1,0.10-13 | 13,00 | |
| H2O | OH- | 1,8.10-16 | 15,74 |
y para las bases:
| Fuerza | Base | Ácido conjugado | Kb | pKb |
Bases
fuertes | Li(OH), K(OH) | Li+ , K+ | - | - |
| Na(OH) | Na+ | - | - | |
| Ca(OH)2 | Ca+2 | - | - | |
| Ba(OH)2 | Ba+2 | - | - | |
bases
débiles | ||||
| CO3-2 | HCO3- | 1,7.10-4 | 3,77 | |
| CN- | HCN | 2,0. 10-5 | 4,69 | |
| NH3 | NH4+ | 1,8. 10-5 | 4,75 | |
| N2H4 | N2H5+ | 9,0. 10-7 | 6,05 | |
bases
muy débiles | ||||
| NH2OH | NH3OH+ | 1,0. 10-9 | 9,00 | |
| C6H5NH2 | C6H5NH3+ | 3,8. 10-10 | 9,42 |
de las dos tablas anteriores se puede observar fácilmente que a medida que un ácido es más fuerte, su base conjugada será más débil y viceversa, si un ácido es muy débil, su base conjugada será muy fuerte.
La teoría de Brönsted ‑ Lowry también tiene sus limitaciones, ya que hay sustancias con un comportamiento típicamente ácido y que no poseen átomos de hidrógeno.
10.1. Efecto inductivo:
Es un desplazamiento parcial del par electrónico de un enlace sencillo “s” hacia el átomo más electronegativo provocando fracciones de carga.
A pesar del que el hidrógeno aporta levemente al carbono su par electrónico, por convenio, se toma como punto de referencia (no provoca efecto inductivo). Así, podemos clasificar los grupos en dos tipos:
- Grupos que retiran electrones. Ejemplos: –NO2, – COOH, – X (halógeno), –OH...
- Grupos que aportan electrones (más que el hidrógeno). Ejemplos: –CH3, –CH2–CH3, –CH(CH3)2, –C(CH3)3, –COO–, –O–...
10.2. Efecto mesómero o resonancia:Es un desplazamiento del par de electrones “p” del doble enlace hacia uno de los átomos por la presencia de pares electrónicos cercanos.
Se produce cuando hay enlace múltiples y la posibilidad de que los e– se deslocalicen (átomo electronegativo con posibilidad de tener parejas de e– sin compartir). A mayor número de formas resonantes mayor estabilidad.
Ejemplo: CH2=CH–CH=CH2
+CH2–CH=CH–CH2– 

–CH2–CH=CH–CH2+
Los tres enlaces C–C son intermedios entre simples y dobles.
Al igual que en el efecto inductivo, existe dos tipos de efectos mesómeros:
Los tres enlaces C–C son intermedios entre simples y dobles.
Al igual que en el efecto inductivo, existe dos tipos de efectos mesómeros:
+M: Se produce por la cesión de un par de e– sin compartir del átomo unido al carbono formándose un doble enlace.

–CHO, –NO, –CN, –CO–CH3, –COOH...

11. PROPIEDADES Y REACCIONES DE LOS ALCANOS
Los alcanos con menos átomos de carbono son gases. El pentano ya es líquido a temperatura ambiente. A medida que el peso molecular aumenta, su punto de fusión aumenta y también su punto de ebullición y su densidad (en el caso de líquidos).
Una ramificación hace descender el punto de ebullición en unos 8‑10 ºC, (los isómeros tienen puntos de ebullición diferentes).
Los ciclo alcanos (CnH2n) tienen propiedades similares a los hidrocarburos del mismo número de átomos de carbono, aunque su punto de ebullición es algo superior.
Los hidrocarburos saturados son especialmente inertes en la mayoría de las reacciones químicas. No obstante reaccionan con halógenos a elevadas temperaturas y con ayuda de catalizadores dando lugar a derivados halogenados. La reacción no conduce a un único derivado halogenado sino a varios:
CH4 + Cl2  CH3Cl + CH2Cl2 + CHCl3 + CCl4
CH3Cl + CH2Cl2 + CHCl3 + CCl4
En condiciones severas de presión y temperatura, los hidrocarburos de alto peso molecular se rompen en fragmentos más pequeños. Este proceso se llama "cracking" y es de mucho interés para la obtención de la gasolina (octano) a partir de hidrocarburos de mayor número de átomos de carbono.
Pero la reacción por excelencia de los hidrocarburos es la combustión; se combinan con oxígeno (arden) para dar dióxido de carbono y agua liberando gran cantidad de energía:
CnH2n+2 + (3n+1)/2 O2  n CO2 + (n+1) H2O
n CO2 + (n+1) H2O
Esta reacción constituye la base de todas las aplicaciones de los hidrocarburos como combustibles y sobre ella se basa nuestra economía, salud y bienestar. El calor liberado va aumentando de forma regular al aumentar el número de carbonos del hidrocarburo (unos 660,44 KJ/mol por cada grupo -CH2-. El metano tiene una entalpía de combustión de –886,16 KJ/mol; el etano de –1.569,14 KJ/mol: el propano – 2.219,58 y así sucesivamente, el decano –6.771,60 KJ/mol.
La fuente principal de los hidrocarburos es el petróleo que se encuentra a profundidades variables tanto en sedimentos terrestres como submarinos, sometido a grandes presiones. El petróleo se puede definir como materia orgánica formada fundamentalmente por hidrocarburos líquidos, con otros gaseosos y sólidos en disolución, acompañada muchas veces de agua salada. Se trata de hidrocarburos, desde el metano hasta especies complejas con más de 40 átomos de carbono que no pueden destilarse sin una descomposición previa.
La complejidad y número enorme de especies presentes en el petróleo obliga a considerarlo como un conjunto de fracciones, entendiendo por tales las partes en que prácticamente puede dividirse el petróleo por razón de la distinta volatilidad de los diferentes hidrocarburos que lo componen. Además de hidrocarburos se hallan también presentes compuestos que contienen Oxígeno, Nitrógeno y Azufre.
El producto que mana de los pozos es un líquido más o menos denso, viscoso y negruzco al que acompañan cantidades importantes de gas desorbido al disminuir la presión del yacimiento. En el propio campo petrolífero se priva al "crudo" del agua y los sólidos interpuestos, pero todavía es necesario, frecuentemente, eliminar los gases disueltos, pues hacen peligroso y difícil su transporte. Esta operación se llama estabilización, y se aprovecha para separar los gases de mayor volatilidad.
El crudo estabilizado se trata en las refinerías de acuerdo con el destino que se fije para los productos obtenidos. La cantidad de cada uno de ellos que se obtenga dependerá, en gran medida, de la constitución molecular , o sea, de la "base" del crudo.
El trabajo en la refinería tiene un cuádruple objetivo:
Separar el crudo en varias fracciones acomodadas a las necesidades del mercado (gasolinas, gasóleo, queroseno, parafinas, etc.) a lo que se llama fraccionamiento.
Modificar (generalmente aumentar) las proporciones de las fracciones volátiles, como la gasolina, mediante la operación llamada craqueo, a expensas de las fracciones más pesadas.
Variar la naturaleza de los hidrocarburos componentes de las fracciones volátiles (gasolinas) para elevar su calidad de carburante (su octanaje), mediante el craqueo catalítico (reforming).
El índice de octano u octanaje es una escala que se utiliza para comparar el poder antidetonante de las gasolinas. Los niveles de referencia son el heptano (nivel 0) y el isooctano (nivel 100). Según esto, una gasolina de 95 octanos tiene el mismo poder antidetonante que una mezcla del 95 % de isooctano y el 5% de heptano. Hay gasolinas que superan el nivel 100, es decir son más antidetonantes que el isooctano puro.
Las gasolinas de cadena lineal son más detonantes que las que tienen compuestos ramificados o cíclicos. La adición de algunos compuestos químicos mejora el poder antidetonante de las gasolinas. El más utilizado es el tetraetil plomo. Sin embargo, últimamente se ha determinado que se dejen de utilizar ya que la contaminación consiguiente por plomo es muy peligrosa.
Eliminar de las fracciones los componentes indeseables, proceso al que se llama genéricamente refino y especialmente desulfuración, desparafinado, desalfaltado, etc.
Existen otras dos fuentes de hidrocarburos que, aunque menos importantes que el petróleo, son dignas de mención:
Gas natural: Es una mezcla de hidrocarburos de entre 1 y 8 átomos de carbono. El metano, con un porcentaje de al menos el 80% constituye casi toda la mezcla, y los demás hidrocarburos registran porcentajes decrecientes. El gas natural, conducido por gaseoductos a las ciudades, es el principal componente del gas ciudad. Con frecuencia se separan previamente por licuefacción el propano y el butano que se comercializan en bombonas a presión.
Carbón: El carbón también es un combustible fósil procedente de los restos vegetales de otras épocas geológicas. Si se calienta un trozo de carbón en condiciones adecuadas (proceso que se conoce como destilación seca del carbón), se descompone originando tres productos principales:
Gas de alumbrado (o gas de coquerías): Mezcla constituida por aproximadamente un 50% de Hidrógeno (H2), un 30 % de metano (CH4), un 8% de monóxido de carbono (CO) y cantidades inferiores de otros hidrocarburos, Nitrógeno (N2) y dióxido de carbono (CO2) entre otros. Se utiliza como combustible. Hace muchos años era muy empleado en el gas ciudad pero en la actualidad existe la tendencia de sustituirlo por gas natural ya que es mucho más limpio.
Coque: es el residuo sólido que deja el carbón. Contiene toda la materia mineral del carbón pero principalmente carbono libre. Esto hace que sea un combustible limpio (sin humos) y por lo tanto muy apreciado.
Alquitrán: líquido negro y viscoso de olor desagradable formado por una mezcla de muchos hidrocarburos aromáticos. Constituye la fuente principal de este tipo de compuestos aromáticos, (ya que en el petróleo y el gas natural predominan los hidrocarburos saturados). Sometido a destilación fraccionada, se pueden separar benceno, tolueno, xileno, naftaleno, fenol, antraceno, etc., también aceites pesados destinados a combustibles en motores diésel y en calefacción, y como residuo una pez negruzca que se utiliza para impermeabilizar edificios y pavimentar carreteras.
El carbón más utilizado es la hulla (producto natural que contiene de entre un 74 y un 90 % de Carbono). La hulla tiene la ventaja de que produce un coque de gran calidad, pero sobre todo porque su alquitrán es una fuente rica en los hidrocarburos aromáticos muy utilizados en la industria química. En la siguiente tabla aparecen los datos de los
productos obtenidos en la destilación seca de la hulla (por cada 1000 Kg):
12. PROPIEDADES DE LOS ALQUENOS | ||||||
La presencia de un doble enlace le da a la molécula una reactividad mucho mayor que la de los alcanos.
12.1. Reacciones de adición al doble enlace:
1.‑ Adición de halógenos:
Por ejemplo:
Esta reacción es muy fácil de realizar a temperatura ambiente y es típica para diferenciar alcanos de alquenos.
2.‑ Adición de hidrácidos:
Por ejemplo:
La adición de los halógenos se verifica por el carbono más sustituido (regla de MarKownikoff):
3.‑ Hidrogenación del doble enlace:
Se realiza con hidrógeno gaseoso y en presencia de un catalizador adecuado, (Níquel si la presión es alta y Platino o Paladio a presiones ordinarias).
12.2. Oxidación del doble enlace:
Es una reacción muy utilizada para conocer la posición del doble enlace. Los agentes oxidantes más utilizados son el ozono (O3), y el permanganato potásico (KMnO4) en medio ácido.
Los alquenos terminales dan el ácido con un carbono menos y CO2:
Los dobles enlaces internos dan dos cetonas (o una cetona y un aldehído):
13. PROPIEDADES DE LOS ALQUINOS
Las reacciones de los alquinos son muy similares a las de los alquenos por ejemplo la adición de Bromo:
No presenta reacciones de adición al doble enlace, pero las reacciones de sustitución si son relativamente fáciles:
14.1. Halogenación:
Estas reacciones se realizan en ausencia de luz y en presencia de un catalizador (suele ser tricloruro de aluminio AlCl3).
Todas estas reacciones de sustitución consisten en la formación de un catión altamente reactivo:
 y luego:
y luego:

con lo que el catalizador se recupera.
14.2. Sulfonación:
Se realiza tratando el benceno con ácido sulfúrico:

14.3. Nitración:
Se realiza tratando el benceno con ácido nítrico:

14.4. Reacción de Friedel‑Crafts:
Es una reacción de sustitución que consiste en la introducción de un grupo alquilo o alconilo en el núcleo bencénico:
 donde X es un halógeno que normalmente es el cloro.
donde X es un halógeno que normalmente es el cloro.
Puede ser que en las reacciones de sustitución no intervenga el benceno sino uno de sus derivados como el tolueno, el nitrobenceno, etc. En estos casos, una nueva reacción de nitración o sulfonación por ejemplo, ¿introduce el grupo sustituyente en cualquier posición o hay alguna preferencia?.
Dependiendo del sustituyente que ya tenga el benceno, éste atraerá hacia él o repelerá los electrones deslocalizados del anillo bencénico, por lo que el resto de los átomos de carbono tendrán una mayor o menor densidad de carga electrónica, por ejemplo:
 Entonces en el caso del tolueno y el fluorobenceno al tener los carbonos situados en orto y para mayor densidad de carga electrónica el catión atacante tendrá mayor preferencia por estas posiciones y en el caso del nitrobenceno ocurrirá lo contrario. Vamos a verlo con algunos ejemplos:
Entonces en el caso del tolueno y el fluorobenceno al tener los carbonos situados en orto y para mayor densidad de carga electrónica el catión atacante tendrá mayor preferencia por estas posiciones y en el caso del nitrobenceno ocurrirá lo contrario. Vamos a verlo con algunos ejemplos:
si hacemos reaccionar el tolueno con ácido nítrico, las sustituciones irán con mayor preferencia a las posiciones “– orto” y “– para”:
Estas reacciones se realizan en ausencia de luz y en presencia de un catalizador (suele ser tricloruro de aluminio AlCl3).
Todas estas reacciones de sustitución consisten en la formación de un catión altamente reactivo:
con lo que el catalizador se recupera.
14.2. Sulfonación:
Se realiza tratando el benceno con ácido sulfúrico:
14.3. Nitración:
Se realiza tratando el benceno con ácido nítrico:
14.4. Reacción de Friedel‑Crafts:
Es una reacción de sustitución que consiste en la introducción de un grupo alquilo o alconilo en el núcleo bencénico:
Puede ser que en las reacciones de sustitución no intervenga el benceno sino uno de sus derivados como el tolueno, el nitrobenceno, etc. En estos casos, una nueva reacción de nitración o sulfonación por ejemplo, ¿introduce el grupo sustituyente en cualquier posición o hay alguna preferencia?.
Dependiendo del sustituyente que ya tenga el benceno, éste atraerá hacia él o repelerá los electrones deslocalizados del anillo bencénico, por lo que el resto de los átomos de carbono tendrán una mayor o menor densidad de carga electrónica, por ejemplo:
si hacemos reaccionar el tolueno con ácido nítrico, las sustituciones irán con mayor preferencia a las posiciones “– orto” y “– para”:
15. POLÍMEROS DE ADICIÓN
Un grupo de aplicación industrial de gran interés en la química de los alquenos, lo constituye la formación de los polímeros de adición. Un polímero de adición puede definirse como una gran molécula formada por la adición de un elevado número de moléculas simples (monómeros) de uno o más alquenos por rotura de dobles enlaces. Por ejemplo, el polietileno se obtiene por polimerización del etileno (eteno), cuya reacción global es:
Existen muchas maneras de realizar la polimerización del etileno. Todas ellas llevan a un mismo grupo que se repite y sólo difieren en la naturaleza de los grupos terminales y en el valor de "n" que puede ir desde 5000 hasta varios millones, con una consistencia que va desde ceras hasta la de productos muy duros y rígidos.
Estos polímeros son muy inertes a los agentes químicos, aunque es algo sensible a la oxidación provocada por rayos ultravioleta. Se emplea como aislante en la industria eléctrica, fabricación de botellas, juguetes, tejidos, etc.
Otros polimeros muy conocidos son los siguientes:
El teflón se obtiene por polimerización del tetrafluoretileno (CF2 = CF2), que es el plástico más resistente a los agentes químicos que se conoce por la fuerza del enlace C‑F. Se utiliza fundamentalmente para revestimientos de metal de los utensilios de cocina.
El polimetacrilato de metilo se obtiene por polimerización de metacrilato de metilo que es un polímero con excelentes propiedades ópticas. Se vende bajo nombres comerciales de Lucite, Plexiglas y Perspex.
El buna se obtiene de la polimerización del 1,3 butadieno que se utiliza para la fabricación del caucho sintético.
La baquelita es una resina sintética obtenida por condensación de un fenol con el aldehído fórmico y que se emplea como sucedáneo del ámbar y del carey (materia córnea sacada del caparazón de algunas tortugas utilizada en marquetería y otras artes decorativas).
No todos los polímetros son sintéticos. Muchos compuestos naturales también lo son, por ejemplo, la seda, la lana, los almidones, la celulosa del algodón, las resinas, el caucho natural y hasta la propia la madera.
16. PROPIEDADES DE LOS ALCOHOLES
Los alcoholes de menos número de carbono son solubles en agua debido a la polaridad del grupo oxidrilo:

al ir aumentando el peso molecular, la solubilidad va disminuyendo, dado que el resto de la cadena no es polar (por la escasa diferencia de electronegatividad que hay entre el C y el H y la simetría de los enlaces tal y como se comentó en el tema anterior).
El punto de ebullición va aumentando a medida que aumenta el número de átomos de carbono de la cadena. Los alcoholes de menos átomos de carbono (metanol, etanol), tienen puntos de ebullición anormalmente altos debido a los enlaces por puentes de hidrógeno:

En los alcoholes podemos distinguir dos tipos de enlaces:

el enlace R‑O y el enlace O‑H. Según cuál de los dos se rompa dará lugar a tipos diferentes de reacciones:
Rotura del enlace O‑H: Es el caso menos frecuente. Se produce en presencia de un metal alcalino obteniéndose un compuesto iónico denominado alcóxido. Por ejemplo:
 al CH3ONa se le llama metóxido sódico.
al CH3ONa se le llama metóxido sódico.
Rotura del enlace R‑O: Hay varios tipos de ellas. Por ejemplo:
Sustitución:
 es una reacción muy empleada para la obtención de derivados halogenados.
es una reacción muy empleada para la obtención de derivados halogenados.
Reacciones de deshidratación en las que se pierde agua durante el proceso:
 los agentes deshidratantes más utilizados son el ácido sulfúrico (H2SO4), el bisulfato sódico (NaHSO4) y el ácido fosfórico (H3PO4). Un ejemplo concreto puede ser:
los agentes deshidratantes más utilizados son el ácido sulfúrico (H2SO4), el bisulfato sódico (NaHSO4) y el ácido fosfórico (H3PO4). Un ejemplo concreto puede ser:

Reacciones de oxidación con agentes inorgánicos como el ion permanganato o el ion dicromato:
con alcoholes primarios se obtiene el ácido correspondiente (pasando por el aldehído como producto intermedio):
 y si el alcohol es secundario, se obtiene la cetona correspondiente:
y si el alcohol es secundario, se obtiene la cetona correspondiente:
 Si el alcohol es ternario, no se produce la reacción en condiciones normales:
Si el alcohol es ternario, no se produce la reacción en condiciones normales:

Reacciones de obtención de alcoholes:
Hidrólisis de halogenuros de alquilo: Esta reacción se produce en presencia de catalizadores básicos:

Hidratación de alquenos: Estas reacciones están catalizadas por ácidos:
 en esta ejemplo, da igual, pero recuerda que, aplicando la regla de Marcownikoff, el grupo OH se une al carbono más sustituido.
en esta ejemplo, da igual, pero recuerda que, aplicando la regla de Marcownikoff, el grupo OH se une al carbono más sustituido.
Fermentación de líquidos azucarados: Por ejemplo, el etanol o alcohol etílico (que es el "alcohol" del lenguaje vulgar), constituyente embriagante de las bebidas alcohólicas, se obtiene por la fermentación de azúcares por la acción de levaduras:

17. REACCIONES DE LOS ALDEHIDOS Y CETONAS
Los aldehídos y las cetonas son compuestos generalmente líquidos si tienen bajo peso molecular. En este caso se disuelven muy bien en agua debido a la polaridad del enlace del grupo carbonilo.
17.1. Reacciones de obtención: Como ya hemos comentado, los aldehídos y las cetonas se obtienen por oxidación de alcoholes catalizado por agentes químicos:
si el alcohol es primario se obtiene el aldehído correspondiente:
 recordemos que en este tipo de reacciones también se puede obtener el ácido correspondiente.
recordemos que en este tipo de reacciones también se puede obtener el ácido correspondiente.

si el alcohol es secundario se obtiene la cetona correspondiente:

Los alcoholes ternarios no presentan este tipo de reacciones.
17.2. Reacciones de adición: Consisten en el ataque al grupo carbonilo (-C=O) por parte de un reactivo nucleófilo, generalmente un anión, por ejemplo:
 se rompe el doble enlace del oxígeno, uniéndose el oxígeno al hidrógeno y el carbono al resto del grupo. Otro ejemplo sería:
se rompe el doble enlace del oxígeno, uniéndose el oxígeno al hidrógeno y el carbono al resto del grupo. Otro ejemplo sería:

17.3. Reacciones de condensación: se verifican en presencia de un catalizador básico fuerte:

17.4. Reacciones oxidación‑reducción: Se observan diferencias entre los aldehídos y las cetonas.
El punto de ebullición va aumentando a medida que aumenta el número de átomos de carbono de la cadena. Los alcoholes de menos átomos de carbono (metanol, etanol), tienen puntos de ebullición anormalmente altos debido a los enlaces por puentes de hidrógeno:
el enlace R‑O y el enlace O‑H. Según cuál de los dos se rompa dará lugar a tipos diferentes de reacciones:
Rotura del enlace O‑H: Es el caso menos frecuente. Se produce en presencia de un metal alcalino obteniéndose un compuesto iónico denominado alcóxido. Por ejemplo:
Rotura del enlace R‑O: Hay varios tipos de ellas. Por ejemplo:
Sustitución:
Reacciones de deshidratación en las que se pierde agua durante el proceso:
Reacciones de oxidación con agentes inorgánicos como el ion permanganato o el ion dicromato:
MnO4- , Cr2O7-2
Reacciones de obtención de alcoholes:
Hidrólisis de halogenuros de alquilo: Esta reacción se produce en presencia de catalizadores básicos:
Hidratación de alquenos: Estas reacciones están catalizadas por ácidos:
Fermentación de líquidos azucarados: Por ejemplo, el etanol o alcohol etílico (que es el "alcohol" del lenguaje vulgar), constituyente embriagante de las bebidas alcohólicas, se obtiene por la fermentación de azúcares por la acción de levaduras:
Los aldehídos y las cetonas son compuestos generalmente líquidos si tienen bajo peso molecular. En este caso se disuelven muy bien en agua debido a la polaridad del enlace del grupo carbonilo.
17.1. Reacciones de obtención: Como ya hemos comentado, los aldehídos y las cetonas se obtienen por oxidación de alcoholes catalizado por agentes químicos:
si el alcohol es primario se obtiene el aldehído correspondiente:
si el alcohol es secundario se obtiene la cetona correspondiente:
Los alcoholes ternarios no presentan este tipo de reacciones.
17.2. Reacciones de adición: Consisten en el ataque al grupo carbonilo (-C=O) por parte de un reactivo nucleófilo, generalmente un anión, por ejemplo:
17.3. Reacciones de condensación: se verifican en presencia de un catalizador básico fuerte:
17.4. Reacciones oxidación‑reducción: Se observan diferencias entre los aldehídos y las cetonas.
Mientras que las cetonas son bastante estables a la oxidación:
En contrapartida, la reducción es sencilla tanto para aldehídos como para cetonas utilizando hidrógeno y un catalizador (platino).
Sustancias de interés
el metanal o formaldehído: También llamado vulgarmente formol se utiliza como antiséptico, como punto de partida para la fabricación de otros compuestos orgánicos y para la preparación de resinas sintéticas.
Las disoluciones de formol también se utilizan para conservar y endurecer muestras de tejidos y órganos.
Como gas también se emplea para desinfectar habitaciones y locales, ya que destruye formas de vida inferiores.
La propanona o acetona: Es un líquido incoloro de olor agradable miscible totalmente en agua, metanol y éter etílico. Se utiliza principalmente como disolvente de muchas sustancias orgánicas (pinturas, esmaltes, etc.).
18. REACCIONES DE LOS ÁCIDOS CARBOXÍLICOS
Los ácidos de pocos átomos de carbono son solubles en agua y poseen un olor desagradable. Los de más bajo peso molecular tienen puntos de ebullición elevados comparados con los que poseen otras sustancias de peso molecular parecido debido a los enlaces por puente de hidrógeno, que hasta incluso hacen que las moléculas de ácido se puedan dimerizar:
| Fórmula | Nombre | pKa |
| HCOOH | Ac. fórmico | 3'75 |
| CH3 ‑ COOH | Ac. acético | 4'75 |
| CH3 ‑ CH2 ‑ COOH | Ac. propiónico | 4'87 |
| CH3 ‑ CH2 ‑ CH2 ‑ COOH | Ac. butírico | 4'81 |
Reacciones de neutralización:
Reacciones de formación de ésteres: Se pueden catalogar también como reacciones de neutralización actuando el alcohol como una base:
Formación de cloruros de ácido:
Sustancias de interés
Ácido fórmico (HCOOH): Se encuentra en las hormigas y en las ortigas. El dolor de las picaduras de abejas, avispas, medusas, pólipos etc. es debido a dicho ácido.
Ácido acético (CH3‑COOH): Es muy importante industrialmente ya que se emplea para obtener acetato de celulosa, que se utiliza para la producción de películas fotográficas y cinematográficas ininflamables, vidrio inastillable, lacas y barnices. También es el responsable de la acidez del vinagre.
19. REACCIONES DE LOS ÉSTERES
La única reacción importante de los ésteres es su hidrólisis en medio básico
con agua para dar el ácido y el alcohol correspondiente:
 como puedes observar, es la reacción inversa a la formación de ésteres, ya que son reacciones de equilibrio.
como puedes observar, es la reacción inversa a la formación de ésteres, ya que son reacciones de equilibrio.
con álcalis para dar la sal y el alcohol correspondiente:
 Un ejemplo particular de este tipo de reacciones es la llamada saponificación de grasas. Dicho proceso consiste en la reacción de hidrólisis de grasas (que son, como ya hemos indicado, poliésteres) con álcalis fuertes, para la producción de ácidos grasos y jabón (sal sódica). Por ejemplo:
Un ejemplo particular de este tipo de reacciones es la llamada saponificación de grasas. Dicho proceso consiste en la reacción de hidrólisis de grasas (que son, como ya hemos indicado, poliésteres) con álcalis fuertes, para la producción de ácidos grasos y jabón (sal sódica). Por ejemplo:

20. REACCIONES DE LAS AMINAS
con álcalis para dar la sal y el alcohol correspondiente:
20. REACCIONES DE LAS AMINAS
Las de peso molecular bajo son líquidas y de olor desagradable. Son muy solubles en disolventes orgánicos pero no en disolventes iónicos o polares como el agua.
Su principal característica es que tienen un marcado carácter básico (como el amoniaco del que provienen). Por ejemplo:

Reacciones de obtención de aminas: Mediante la síntesis de Hoffman se pueden obtener los tres tipos de aminas. El proceso consiste en calentar un halogenuro de alquilo en una disolución alcohólica de amoniaco:
 donde X es un halógeno.
donde X es un halógeno.
Por otra parte las aminas aromáticas son de fácil obtención por reducción del nitrobenceno:
 el compuesto obtenido en este último ejemplo se denomina el aminobenceno, el fenilamino o "vulgarmente" la anilina.
el compuesto obtenido en este último ejemplo se denomina el aminobenceno, el fenilamino o "vulgarmente" la anilina.
Reacciones de basicidad: Los cloruros de ácido con las aminas dan lugar a las amidas que veremos a continuación. Un ejemplo de este tipo de reacciones es el siguiente:

21. REACCIONES DE LAS AMIDAS
Su principal característica es que tienen un marcado carácter básico (como el amoniaco del que provienen). Por ejemplo:
Reacciones de obtención de aminas: Mediante la síntesis de Hoffman se pueden obtener los tres tipos de aminas. El proceso consiste en calentar un halogenuro de alquilo en una disolución alcohólica de amoniaco:
Por otra parte las aminas aromáticas son de fácil obtención por reducción del nitrobenceno:
Reacciones de basicidad: Los cloruros de ácido con las aminas dan lugar a las amidas que veremos a continuación. Un ejemplo de este tipo de reacciones es el siguiente:
Una de las aminas más importante es la anilina (fenilamina). Dicha sustancia es la materia prima de obtención de centenares de productos intermedios en la industria de los colorantes.
21. REACCIONES DE LAS AMIDAS
Por reacción de cloruros de ácido con aminas como ya hemos visto en el apartado anterior:

Por deshidratación de sales amónicas orgánicas: por ejemplo:

Sustancias de interés
La urea: Es el primer compuesto "orgánico" que se sintetizó en un laboratorio (1828). La urea o carbamida H2N‑CO‑NH2, es el derivado más importante del ácido carbónico. Es el producto final del metabolismo de las proteínas en todos los animales. Una persona adulta, por ejemplo, excreta unos 30 gr de urea al día en la orina, de donde se aisló por primera vez en 1773.
A escala industrial se obtiene por reacción del amoniaco con dióxido de carbono a 150ºC y 350 atm de presión según la reacción:
 Se utiliza como fertilizante, como complemento proteínico en el forraje del ganado y en la fabricación de plásticos.
Se utiliza como fertilizante, como complemento proteínico en el forraje del ganado y en la fabricación de plásticos.
El nylón: Es un fibra poliamídica que se produce en la condensación de una diamida y un ácido dicarboxílico. Entre este tipo de fibras cabe destacar el nylón‑66 (66 quiere decir que está formada por una diamida de 6 átomos de carbono y un ácido dicarboxílico de 6 átomos de carbono:

La poliamida, con una masa molecular entre 10000 y 25000, funde a unos 250ºC y el material fundido puede ser estirado en finos hilos. Estos hilos sometidos, a temperatura ambiente, a una tensión que los alarga hasta una longitud 4 veces superior, a diferencia de los materiales elásticos, no se contrae cuando cesa la tensión, transformándose en este proceso de estiramiento en un material fibroso que posee mayor resistencia y brillo, y es parecido a la seda natural. Se utiliza para fabricar medias, paracaídas, alfombras y muchos otros artículos.
Por deshidratación de sales amónicas orgánicas: por ejemplo:
Sustancias de interés
La urea: Es el primer compuesto "orgánico" que se sintetizó en un laboratorio (1828). La urea o carbamida H2N‑CO‑NH2, es el derivado más importante del ácido carbónico. Es el producto final del metabolismo de las proteínas en todos los animales. Una persona adulta, por ejemplo, excreta unos 30 gr de urea al día en la orina, de donde se aisló por primera vez en 1773.
A escala industrial se obtiene por reacción del amoniaco con dióxido de carbono a 150ºC y 350 atm de presión según la reacción:
El nylón: Es un fibra poliamídica que se produce en la condensación de una diamida y un ácido dicarboxílico. Entre este tipo de fibras cabe destacar el nylón‑66 (66 quiere decir que está formada por una diamida de 6 átomos de carbono y un ácido dicarboxílico de 6 átomos de carbono:
22. REACCIONES DE LOS NITRILOS
La característica principal de los nitrilos es la polaridad del triple enlace, al igual que ocurre en las cetonas:
La mayoría de los nitrilos son líquidos muy tóxicos.
Reacciones de obtención: Los nitrilos pueden obtenerse por dos caminos diferentes:
Deshidratación de amidas:
Tratando derivados halogenados con cianuro potásico:
Reacción de hidrólisis: Los nitrilos se hidrolizan en medio básico según la reacción:
Sustancias de interés
Cianuro de hidrógeno: también llamado ácido cianhídrico o metanonitrilo es un líquido incoloro muy venenoso, pues la dosis mortal para una persona es de 0'05 mgr. También se emplea como fumigante.Cianuro de vinilo: se utiliza en la fabricación del caucho sintético Buna‑N, que es un copolimetil de este compuesto y butadieno. También se utiliza en la fabricación de fibras poliacrílicas como el orlón.
ANIMACIONES
23. CUESTIONES
24. PRÁCTICAS
25. VÍDEOS
|
|
Vídeo 1
|









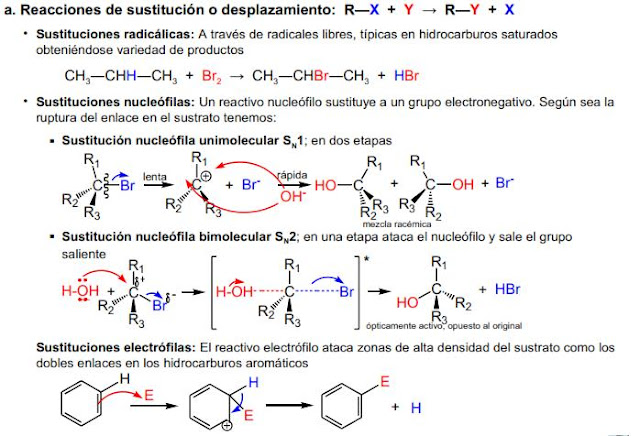























No hay comentarios:
Publicar un comentario